- Автор: Бездітко П. А., Безега Н. М.
- Категорія: Український журнал «Офтальмологія» № 4 (15) 2021
- Опубліковано: 28 грудня 2021
- Перегляди: 3864
https://doi.org/10.30702/Ophthalmology28122021-15.4.12-18/379-008.64
УДК 617.735-02:616.379-008.64]-06-089-036.8
Бездітко П. А.1, д-р мед. наук, завідувач кафедри офтальмології, https://orcid.org/0000-0002-9466-9586
Безега Н. М.2∗, асистент кафедри оториноларингології з офтальмологією
1Харківський національний медичний університет, м. Харків, Україна
2Полтавський державний медичний університет, м. Полтава, Україна
*E-mail: Ця електронна адреса захищена від спам-ботів. Вам потрібно увімкнути JavaScript, щоб побачити її.
Резюме
Мета роботи – виявити особливості післяопераційного періоду у хворих на хронічний дакріоцистит та цукровий діабет 2-го типу (ЦД2) після проведення ендоскопічної ендоназальної дакріоцисториностомії (ЕЕД) залежно від ступеня компенсації ЦД.
Матеріали та методи. У дослідженні брали участь 30 хворих на хронічний дакріоцистит та ЦД2, яким була проведена ЕЕД за стандартною методикою. Хворі були розділені на групи відповідно до ступеня компенсації ЦД2: 6 хворих на компенсований, 7 хворих на субкомпенсований та 17 хворих на декомпенсований ЦД2. Результати операції оцінювали через 2 місяці, 6 місяців та 2 роки. Крім стандартних, методи офтальмологічного дослідження включали сльозо-носову пробу, промивання сльозовивідних шляхів, ендоскопічне дослідження порожнини носа.
Результати та їх обговорення. Ефективність ЕЕД при декомпенсованому ЦД2 через 2 місяці (58,8 ± 11,9 % хворих) в середньому в 1,4 раза, через 6 місяців (52,9 ± 12,1 % хворих) та 2 роки (41,2 ± 11,9 % хворих) – у 1,5 раза була меншою, ніж при субкомпенсованому та компенсованому ЦД2 (р < 0,05). У хворих на декомпенсований ЦД2 сльозотеча відзначалася у 41,2 ± 11,9 % хворих через 2 місяці, у 47,1 ± 12,1 % хворих через 6 місяців та у 58,8 ± 11,9 % хворих через 2 роки після проведення операції, що було в середньому у 2,7, 2,1 та 1,5 раза відповідно частіше, ніж при субкомпенсованому та компенсованому ЦД2 (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05).
Висновок. Особливості післяопераційного періоду у хворих на хронічний дакріоцистит після проведення ЕЕД залежать від ступеня компенсації ЦД2. Ефективність ЕЕД при декомпенсованому ЦД2 через 2 місяці в середньому в 1,4 раза, через 6 місяців та 2 роки – у 1,5 раза є меншою, ніж при субкомпенсованому та компенсованому ЦД2.
Ключові слова: цукровий діабет 2-го типу, ступінь компенсації цукрового діабету, хронічний дакріоцистит, ефективність ендоскопічної ендоназальної дакріоцисториностомії, особливості післяопераційного періоду.
Вступ
Захворюваність на цукровий діабет (ЦД) щороку зростає. Прогнозується, що до 2030 року кількість хворих на ЦД збільшиться до 552 млн, а до 2040 року досягне 642 млн [1, 2]. На ЦД хворіє 11,1–24,3 % хворих з непрохідністю сльозовивідних шляхів, які потребують хірургічного лікування [3, 4]. Літературні дані свідчать про те, що у хворих на ЦД зрощення отвору риностоми рубцевою чи грануляційною тканиною відбувається частіше, ніж у загальній популяції [3–8]. Дакріоцистит є причиною порушення відведення сльози не менше, ніж у третині випадків [9]. Найбільш ефективним методом лікування хронічного дакріоциститу є ендоскопічна ендоназальна дакріоцисториностомія (ЕЕД). Проте у літературі відсутня інформація щодо особливостей післяопераційного періоду у хворих на хронічний дакріоцистит та ЦД після проведення ЕЕД залежно від ступеня компенсації ЦД.
Мета роботи – виявити особливості післяопераційного періоду у хворих на хронічний дакріоцистит та цукровий діабет 2-го типу (ЦД2) залежно від ступеня компенсації ЦД.
Матеріали та методи
У дослідженні брали участь 30 хворих на хронічний дакріоцистит та ЦД2 (19 жінок та 11 чоловіків), яким була проведена ЕЕД за стандартною методикою. Тривалість ЦД2 до 5 років відзначали у 7 хворих основної групи, 5–10 років – в 11, понад 10 років – у 12 хворих. Вік хворих в середньому становив 66,5 ± 9,5 року, коливався від 41 до 82 років. Хворі були розділені на групи відповідно до ступеня компенсації ЦД2: 6 хворих на компенсований (НвА1с < 7,1 %), 7 хворих на субкомпенсований (НвА1с – 7,1–7,5 %) та 17 хворих на декомпенсований ЦД2 (НвА1с > 7,5 %). Передопераційна підготовка, хід операції та тактика післяопераційного ведення хворих в усіх групах була стандартною, не відрізнялась одна від одної. Для проведення ЕЕД використовували стандартний набір інструментів: операційний мікроскоп фірми «Opton» (Німеччина), ендоскопічну відеосистему NET-260SLCB фірми Mega Medical Co., Ltd. (Південна Корея), 4,0 мм жорсткі ендоскопи фірми Risingmed та ShenDa (Китай), аспіраційну систему, шейверну систему зі змінними бор-насадками (фірми «Storz» і «Елепс»).
Тривалість спостереження становила 2 роки, результати операції оцінювали через 2 місяці, 6 місяців та 2 роки. ЕЕД вважали ефективним методом лікування при відновленні вільного пасивного сльозовідведення під час промивання сльозових шляхів, зникнення сльозотечі та відсутності повторного інфікування сльозового мішка.
Крім стандартних (візометрії, зовнішнього огляду, біомікроскопії, тонометрії, офтальмоскопії), методи офтальмологічного дослідження включали сльозо-носову пробу, промивання сльозовивідних шляхів, ендоскопічне дослідження порожнини носа.
Для оцінювання числових показників використовували середнє арифметичне значення (M) та стандартне відхилення (m). При порівняльному аналізі міжгрупових порядкових показників застосовували непараметричний метод для незалежних вибірок (ранговий критерій Манна – Уітні). Для порівняння структури груп у відсотках (P % ± m %) у різні терміни спостереження використовували критерій χ2. Усі результати оцінювали при граничному рівні похибки не більше 5 % (р < 0,05).
Результати та їх обговорення
Компенсований ЦД2 був виявлений у 20 ± 7,3 % хворих, субкомпенсований – у 23,3 ± 7,7 %, декомпенсований – у 56,7 ± 9,1 % хворих.
Виявили, що ефективність ЕЕД у хворих на хронічний дакріоцистит залежить від ступеня компенсації ЦД2: зменшується при декомпенсованому ЦД2 в усі терміни спостереження (р < 0,05). Так, через 2 місяці після проведення ЕЕД операція була ефективною у 58,8 ± 11,9 % хворих на декомпенсований ЦД2 (10 осіб), що було, в середньому, у 1,4 раза менше, ніж при субкомпенсованому (85,7 ± 13,2 %, 6 хворих) та компенсованому ЦД2 (83,3 ± 15,2 %, 5 хворих) (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05). Через 6 місяців операція виявилася ефективною у 52,9 ± 12,1 % хворих на декомпенсований ЦД2 (9 осіб), що було в середньому у 1,5 раза менше, ніж при субкомпенсованому (71,4 ± 17,0 %, 5 хворих) та компенсованому ЦД2 (83,3 ± 15,2 %, 5 хворих) (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05). Через 2 роки операція виявилася ефективною у 41,2 ± 11,9 % хворих на декомпенсований ЦД2 (7 осіб), що було в середньому у 1,5 раза менше, ніж при субкомпенсованому (57,1 ± 18,7 %, 4 хворих) та компенсованому ЦД2 (66,7 ± 19,2 %, 4 хворих) (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05), як це показано на рисунку 1.
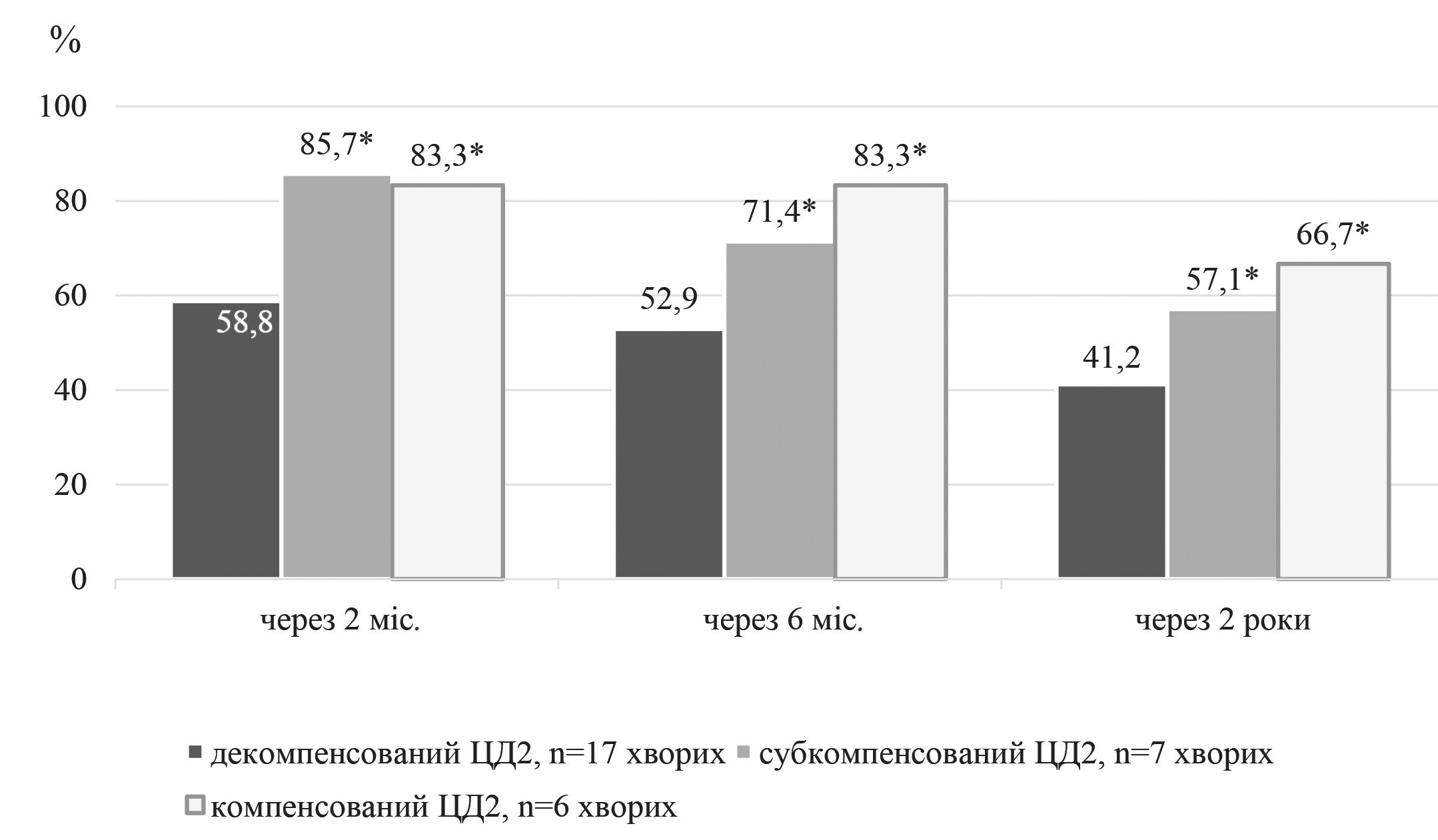
Примітка.* – оцінка статистичної значущості відмінностей між групою хворих на декомпенсований ЦД2 та іншими групами в цей період спостереження р < 0,05.
Відзначили залежність наявності основних симптомів захворювання у хворих на хронічний дакріоцистит від ступеня компенсації ЦД2 після проведення ЕЕД в усі терміни спостереження, р < 0,05 (рисунок 2). Через 2 місяці після проведення операції сльозотеча відзначалася у 41,2 ± 11,9 % хворих на декомпенсований ЦД2 (7 осіб), що було в середньому у 2,7 раза частіше, ніж при субкомпенсованому (14,3 ± 13,2 %, 1 хворий) та компенсованому ЦД2 (16,7 ± 15,2 %, 1 хворий) (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05); злипання повік, набряк медіального канту та біль біля внутрішнього кута ока були виявлені тільки у хворих на декомпенсований ЦД2, відзначалися в 11,8 ± 7,8 % хворих (2 осіб), 5,9 ± 5,7 % хворих (1 особа), 5,9 ± 5,7 % хворих (1 особа) з 17 хворих на декомпенсований ЦД2 відповідно.
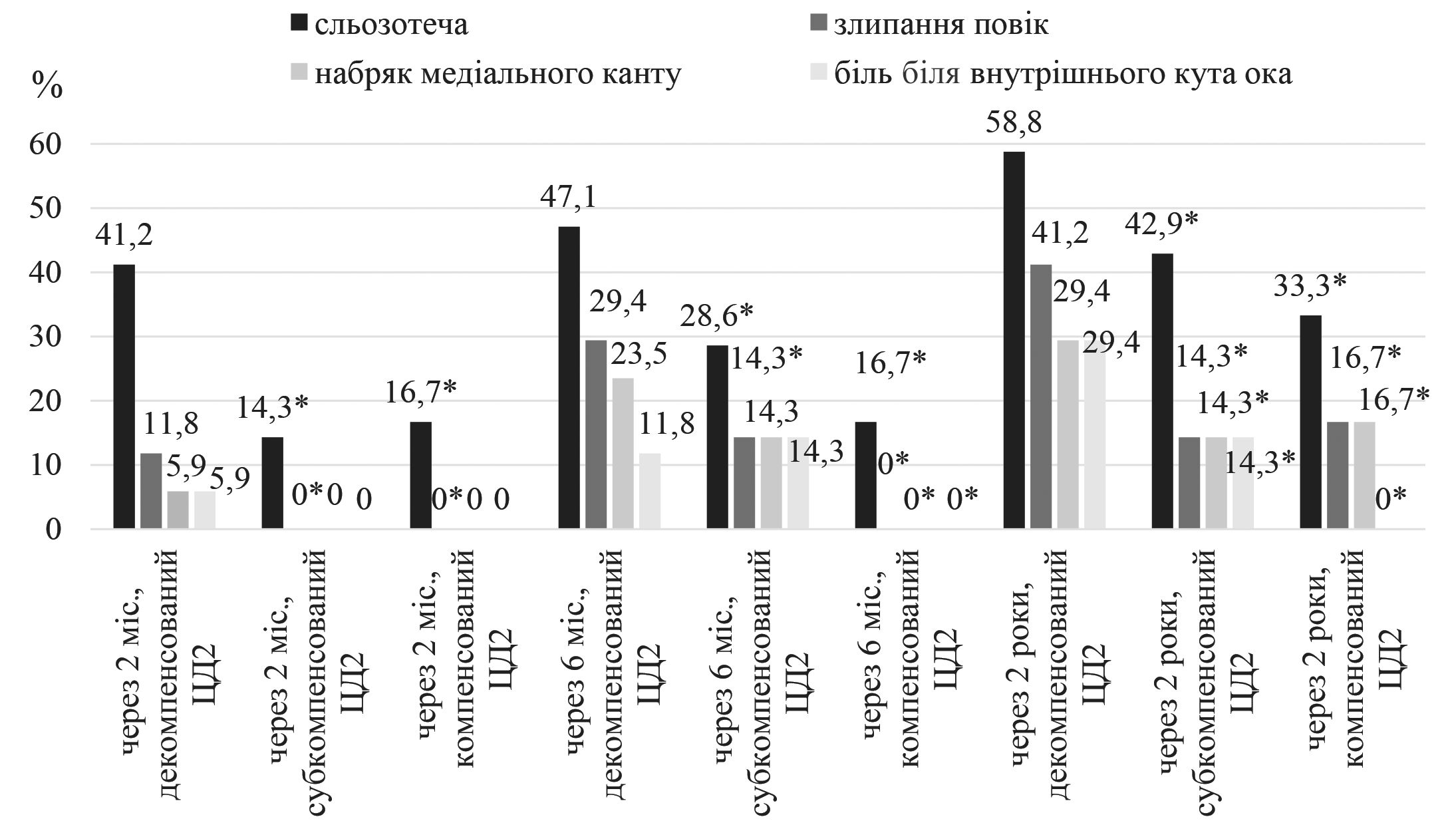
Примітка.* – оцінка статистичної значущості відмінностей між групою хворих на декомпенсований ЦД2 та іншими групами в цей період спостереження р < 0,05.
Через 6 місяців після проведення операції сльозотеча була виявлена у 47,1 ± 12,1 % хворих на декомпенсований ЦД2 (8 осіб), що було в середньому у 2,1 раза частіше, ніж при субкомпенсованому (28,6 ± 17,1 %, 2 хворих) та компенсованому ЦД2 (16,7 ± 15,2 %, 1 хворий) (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05); злипання повік відзначили у 29,4 ± 11,1 % хворих на декомпенсований ЦД2 (5 осіб), що було у 2,1 раза частіше, ніж при субкомпенсованому ЦД2 (14,3 ± 13,2 %, 1 хворий) (р < 0,05); набряк медіального канту виявили у 23,5 ± 10,3 % хворих на декомпенсований ЦД2 (4 особи), що достовірно не відрізнялося від показника хворих на субкомпенсований ЦД2 (14,3 ± 13,2 %, 1 хворий) (р < 0,05); біль біля внутрішнього кута ока відзначили у 11,8 ± 7,8 % хворих на декомпенсований ЦД2 (2 особи), що достовірно не відрізнялося від показника хворих на субкомпенсований ЦД2 (14,3 ± 13,2 %, 1 хворий) (р > 0,05); у хворих на компенсований ЦД2 злипання повік, набряк медіального канту та біль біля внутрішнього кута ока були відсутні у всіх хворих.
Через 2 роки після проведення операції сльозотеча спостерігалася у 58,8 ± 11,9 % хворих на декомпенсований ЦД2 (10 осіб), що було в середньому у 1,5 раза частіше, ніж при субкомпенсованому (42,9 ± 18,7 %, 3 хворих) та компенсованому ЦД2 (33,3 ± 19,2 %, 2 хворих) (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05); злипання повік відзначили у 41,2 ± 11,9 % хворих на декомпенсований ЦД2 (7 осіб), що було в середньому у 3,8 раза частіше, ніж при субкомпенсованому (14,3 ± 13,2 %, 1 хворий) та компенсованому ЦД2 (16,7 ± 15,2 %, 1 хворий) (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05); набряк медіального канту виявили у 29,4 ± 11,1 % хворих на декомпенсований ЦД2 (5 осіб), що було в середньому у 1,9 раза частіше, ніж при субкомпенсованому (14,3 ± 13,2 %, 1 хворий) та компенсованому ЦД2 (16,7 ± 15,2 %, 1 хворий) (р < 0,05), показники яких достовірно не відрізнялися між собою (р > 0,05); біль біля внутрішнього кута ока спостерігався у 29,4 ± 11,1 % хворих на декомпенсований ЦД2 (5 осіб), що було у 2,1 раза частіше, ніж при субкомпенсованому ЦД2 (14,3 ± 13,2 %, 1 хворий) (р < 0,05), у всіх хворих на компенсований ЦД2 цей симптом був відсутній.
Таким чином, особливості післяопераційного періоду у хворих на хронічний дакріоцистит після проведення ЕЕД залежать від ступеня компенсації ЦД2. Ефективність ЕЕД при декомпенсованому ЦД2 через 2 місяці в середньому в 1,4 раза, а через 6 місяців та 2 роки – у 1,5 раза є меншою, ніж при субкомпенсованому та компенсованому ЦД2.
Високий ризик зрощення отвору риностоми рубцевою чи грануляційною тканиною у хворих на декомпенсований ЦД2 може бути пов’язаний з більш вираженим порушенням загоєння ран, змінами імунної системи, патологією запального процесу [10–12], а також діабетичними змінами мікросудин слизової оболонки носа [6], характерними для декомпенсованого ЦД.
Висновок
Особливості післяопераційного періоду у хворих на хронічний дакріоцистит після проведення ЕЕД залежать від ступеня компенсації ЦД2. Ефективність ЕЕД при декомпенсованому ЦД2 через 2 місяці (58,8 ± 11,9 % хворих) в середньому в 1,4 раза, через 6 місяців (52,9 ± 12,1 % хворих) та 2 роки (41,2 ± 11,9 % хворих) – у 1,5 раза є меншою, ніж при субкомпенсованому та компенсованому ЦД2.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
- Whiting DR, Guariguata L, Weil C, Shaw J. IDF diabetes atlas: global estimates of the prevalence of diabetes for 2011 and 2030. Diabetes Res Clin Pract. 2011;94(3):311-21. https://doi.org/10.1016/j.diabres.2011.10.029
- Ogurtsova K, da Rocha Fernandes JD, Huang Y, Linnenkamp U, Guariguata L, Cho NH, Cavan D, Shaw JE, Makaroff LE. IDF Diabetes Atlas: Global estimates for the prevalence of diabetes for 2015 and 2040. Diabetes Res Clin Pract. 2017;128:40-50. https://doi.org/10.1016/j.diabres.2017.03.024
- Rabina G, Golan S, Neudorfer M, Leibovitch I. External Dacryocystorhinostomy: Characteristics and Surgical Outcomes in Patients with and without Previous Dacryocystitis. J Ophthalmol. 2013;2013:287524. https://doi.org/10.1155/2013/287524
- Sung JY, Lee YH, Kim KN, Kang TS, Lee SB. Surgical outcomes of endoscopic dacryocystorhinostomy: analysis of age effect. Sci Rep. 2019;9(1):19861. https://doi.org/10.1038/s41598-019-56491-y
- Keren S, Abergel A, Manor A, Rosenblatt A, Koenigstein D, Leibovitch I, Ben Cnaan R. Endoscopic dacryocystorhinostomy: reasons for failure. Eye (Lond). 2020;34(5):948-53. https://doi.org/10.1038/s41433-019-0612-y
- Beldovskaya NY, Karpishchenko SA, Kulikova OA, Baranskaya SV. [About endonasal laser dacryocystorhinostomy unfavorable outcomes]. Oftalmologiceskie vedomosti. 2016;9(2):14-18. Russian. https://doi.org/10.17816/OV9214-18
- Kraiem A, Abdessalem R, Christov T, Ben Romdhane B, Kamoun M. La dacryocysto-rhinostomie chez le diabétique [Dacryocystorhinostomy in diabetics]. Tunis Med. 1986;64(10):873-6. French. PMID: 3824546.
- Goel R, Garg S, Nagpal S, Kumar S, Kamal S. Naso-cutaneous fistula following transcanalicular laser dacrocystorhinostomy. Saudi J Ophthalmol. 2014;28(1):69-71. https://doi.org/10.1016/j.sjopt.2013.11.006
- Cherkunov BF. Bolezni sleznykh organov [Diseases of the lacrimal organs]. Samara; 2001. 296 p. Russian.
- Tsai S, Clemente-Casares X, Revelo XS, Winer S, Winer DA. Are obesity-related insulin resistance and type 2 diabetes autoimmune diseases? Diabetes. 2015;64(6):1886-97. https://doi.org/10.2337/db14-1488
- Velloso LA, Eizirik DL, Cnop M. Type 2 diabetes mellitus--an autoimmune disease? Nat Rev Endocrinol. 2013;9(12):750-5. https://doi.org/10.1038/nrendo.2013.131
- Zhong J, Gong Q, Mima A. Inflammatory Regulation in Diabetes and Metabolic Dysfunction. J Diabetes Res. 2017;2017:5165268. https://doi.org/10.1155/2017/5165268
Стаття надійшла в редакцію 16.11.2021 р. Рецензія на статтю надійшла в редакцію 30.11.2021 р.