- Автор: Super User
- Категорія: №2 (10) 2019
- Опубліковано: 26 грудня 2019
- Перегляди: 4996
УДК 617.7–073.178–617.73
https://doi.org/10.30702/Ophthalmology.2019/10.137686
Веселовська З. Ф., професор, член-кореспондент НАМН України
Веселовська Н. М., професор
Запорожченко І. Б., доцент
Київський медичний університет, Очна клініка КМКЛ № 1, м. Київ, Україна
Резюме. Робота присвячена дослідженню гіпотензивного і нейропротекторного ефекту, а також місцевих побічних реакцій препарату Монопрост порівняно з оригінальним латанопростом з консервантом.
Матеріали та методи. Дві групи пацієнтів з первинною відкритокутовою глаукомою (ПВКГ) були розділені за ознакою терапії. У І групу входило 20 пацієнтів (26 очей), які отримували оригінальний латанопрост з консервантом у вигляді одноразової інстиляції (1 раз на ніч). До ІІ групи – 20 пацієнтів (26 очей), які отримували Монопрост у вигляді одноразової інстиляції (1 раз на ніч). Термін спостереження становив 12 тижнів. Обстеження включало візометрію, периметрію, тонометрію і оптичну когерентну томографію сітківки та зорового нерва.
Результати. Обстеження та спостереження показали високий гіпотензивний ефект Монопросту порівняно з оригінальним латанопростом з БАХ (зниження внутрішньоочного тиску наприкінці дослідження становило 32 % та 29 % відповідно). Застосування препарату Монопрост характеризувалося низьким рівнем місцевих побічних реакцій, призводило до зниження офтальмотонусу в пацієнтів із ПВКГ у середньому на 32 % від початкового рівня. Досягнута гіпотензивна дія при відсутності токсичного впливу консервантів забезпечила ефект непрямої нейропротекції та супроводжувалась позитивною динамікою як гостроти зору, так і показників периметрії та ОКТ. Препарат характеризується низьким рівнем побічних ефектів і може бути рекомендований як гіпотензивний препарат пацієнтам із ПВКГ.
Ключові слова: первинна відкритокутова глаукома, Монопрост, Ксалатан, внутрішньоочний тиск, нейропротекція.
Veselovska Z. F., Veselovska N. M., Zaporozhchenko I. B.
Kyiv Medical University, Eye Clinic of Kyiv City Hospital No 1, Kyiv, Ukraine
Update of Therapeutic Abilities of Pharmacotherapy of Primary Open Angle Glaucoma
Abstract
The aim of research is to study the hypotensive, neuroprotective effects and side effects of Monoprost in comparison with the original preserved latanoprost (Xalatan).
Material and methods. The I group includes 20 patients (26 eyes), who obtained instillations of preserved latanoprost (one dose before night). The II group consists of 20 patients (26 eyes), who used eye drops of Monoprost (one dose before night).
The observation period was 12 weeks. The examination included visual acuity, perimetry, tonometry and optical coherence tomography of the retina and optic nerve.
Results. The examination revealed high hypotensive effect of Monoprost in comparison of the original preserved latanoprost (IOP reduction at the end of the study was 32% and 29%, respectively). Eye drops of Monoprost was characterized by a low level of local side effects, leading to a decrease IOP in patients with POAG by an average of 32% from the initial level. The achieved hypotensive effect and the absence of the toxic effect of preservatives provided the effect of indirect neuroprotection and was accompanied by positive dynamics of both visual acuity and perimetry and OCT data.
The drug is characterized by low level of side effects and may be recommended as a hypotensive drug in patients with primary open-angle glaucoma.
Keywords: primary open-angle glaucoma, Monoprost, Xalatan, intraocular pressure, neuroprotection.
Глаукома є багатофакторною за патогенезом, хронічною за перебігом пожиттєвою патологією, яка проявляється ознаками оптичної нейропатії з характерними змінами диска зорового нерва та поля зору [1]. Внутрішньоочний тиск при цьому є основним модифікованим фактором ризику розвитку та прогресування глаукоми [1, 2].
Первинна відкритокутова глаукома (ПВКГ) – це хронічна прогресуюча оптична нейропатія, яка характеризується морфологічними змінами диска зорового нерва та шару нервових волокон сітківки за відсутності інших захворювань та вроджених аномалій [1].
Із цими змінами пов’язані прогресуюча втрата гангліонарних клітин сітківки та поля зору [1, 2, 6, 22].
Рекомендації останніх років (2017–2018) пропонують використовувати препарати без консервантів у лікуванні глаукоми [1–3, 10, 15, 16, 19]. Згідно з рекомендаціями European Glaucoma Society (2015), при виборі препарату слід звертати увагу на поверхню ока та за потреби віддавати перевагу препаратам без консервантів. У разі ураження поверхні ока рекомендовано користуватися препаратами без консервантів (EMEA public statement on antimicrobial preservatives in ophthalmic preparations for human use (December 2009)) [1, 5].
Препарати без консервантів для лікування глаукоми показані багатьом групам пацієнтів [2, 3, 10, 12–15, 16, 21].
Відповідно до рекомендацій 4-го видання «Термінологія та настанови з глаукоми» Європейського глаукомного товариства (переклад на українську мову та адаптація проф. Веселовської З. Ф., Українське глаукомне товариство), першою лінією терапії є лікування (препарати), затверджене офіційними контролюючими органами, а терапією першого вибору є препарат, якому лікар віддає перевагу на першому етапі лікування для зниження внутрішньоочного тиску (ВОТ). Комбінована терапія не рекомендується як перша лінія терапії [1, 5, 14, 20] (таблиця 1).
Таблиця 1. Рекомендації European Glaucoma Society, 4-е видання (переклад та адаптація проф. Веселовської З. Ф.)
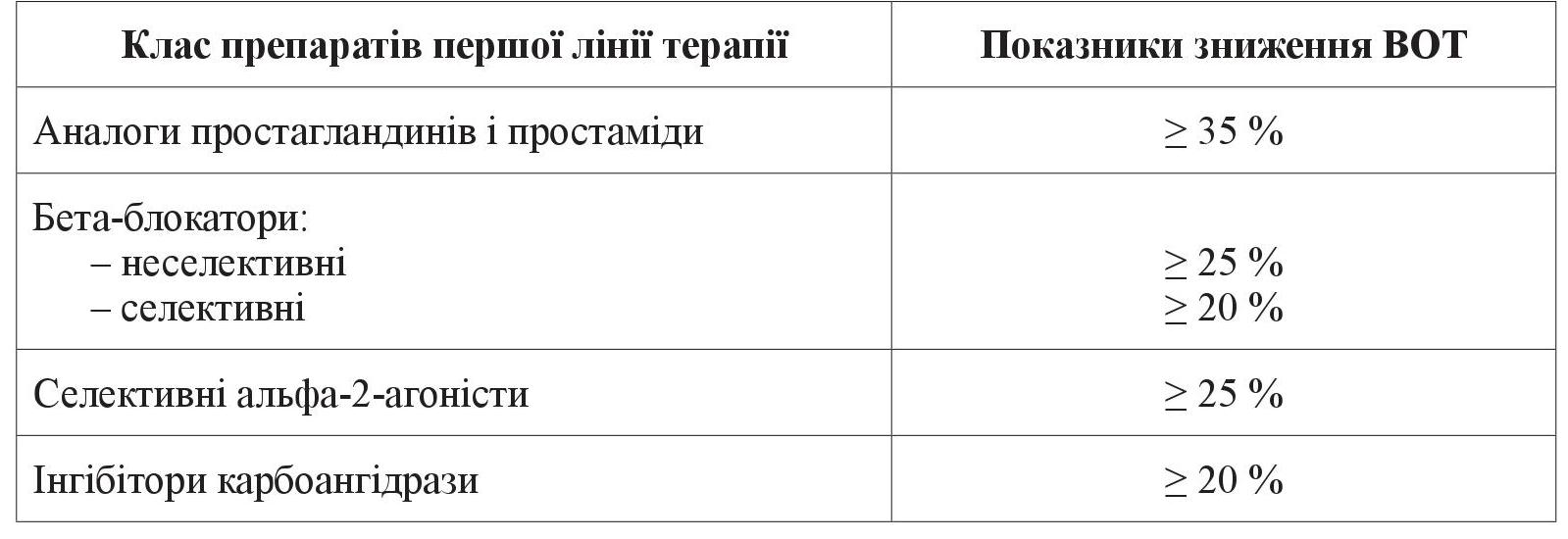
Простагландини, за даними метааналізу, демонструють найвищі показники зниження ВОТ. Найгірший результат серед препаратів першого вибору – в інгібіторів карбоангідрази і селективних бета-блокаторів [1, 8, 9, 13].
Таким чином, простагландини і є препаратами першої лінії терапії, тобто тими препаратами, які рекомендовано обирати як перше призначення для лікування глаукоми з метою зниження ВОТ [1, 8, 9, 13, 15, 16, 21].
Препарат першого вибору – це препарат, якому віддає перевагу лікар з урахуванням як співвідношення ефективності зниження ВОТ і безпеки лікування, так і особливостей пацієнта (з огляду на його супутні захворювання та стан очної поверхні) [1, 8, 9, 11, 20].
Слід відзначити, що для більшості офтальмологів світу препаратами першого вибору вважають простагландини, а лідером серед призначень – препарати на основі молекули латанопросту за даними величезної доказової бази його ефективності і відмінного профілю безпеки [15–18, 21]. На сьогодні єдиною методикою з доведеною ефективністю щодо збереження зорової функції є зниження ВОТ з мінімальними добовими флюктуаціями. За даними численних досліджень, простагландини здатні забезпечити не тільки найбільше зниження рівня ВОТ на 30–35 %, а й мінімальні добові перепади ВОТ у денні та нічні часи, порівняно з іншими групами антиглаукомних крапель [1, 8, 9, 13–18, 21].
Згідно з даними метааналізу, простагландини навіть перевищують інші групи як за ефективністю, так і за рівнем безпеки, і вважаються найкращими. Такі простагландини, як латанопрост, біматопрост, травопрост та тафлупрост, визначені як препарати першої лінії вибору для лікування глаукоми серед решти груп препаратів (рисунок 1). Латанопрост, біматопрост та травопрост мають майже еквівалентну ефективність у зниженні ВОТ, що становить 8–9 мм рт. ст., але за даними Arias 2010, латанопрост серед інших простагландинів має найкращий рівень переносимості, з чим і пов’язана найбільша прихильність до нього в терапії глаукоми [8, 9, 14–16].
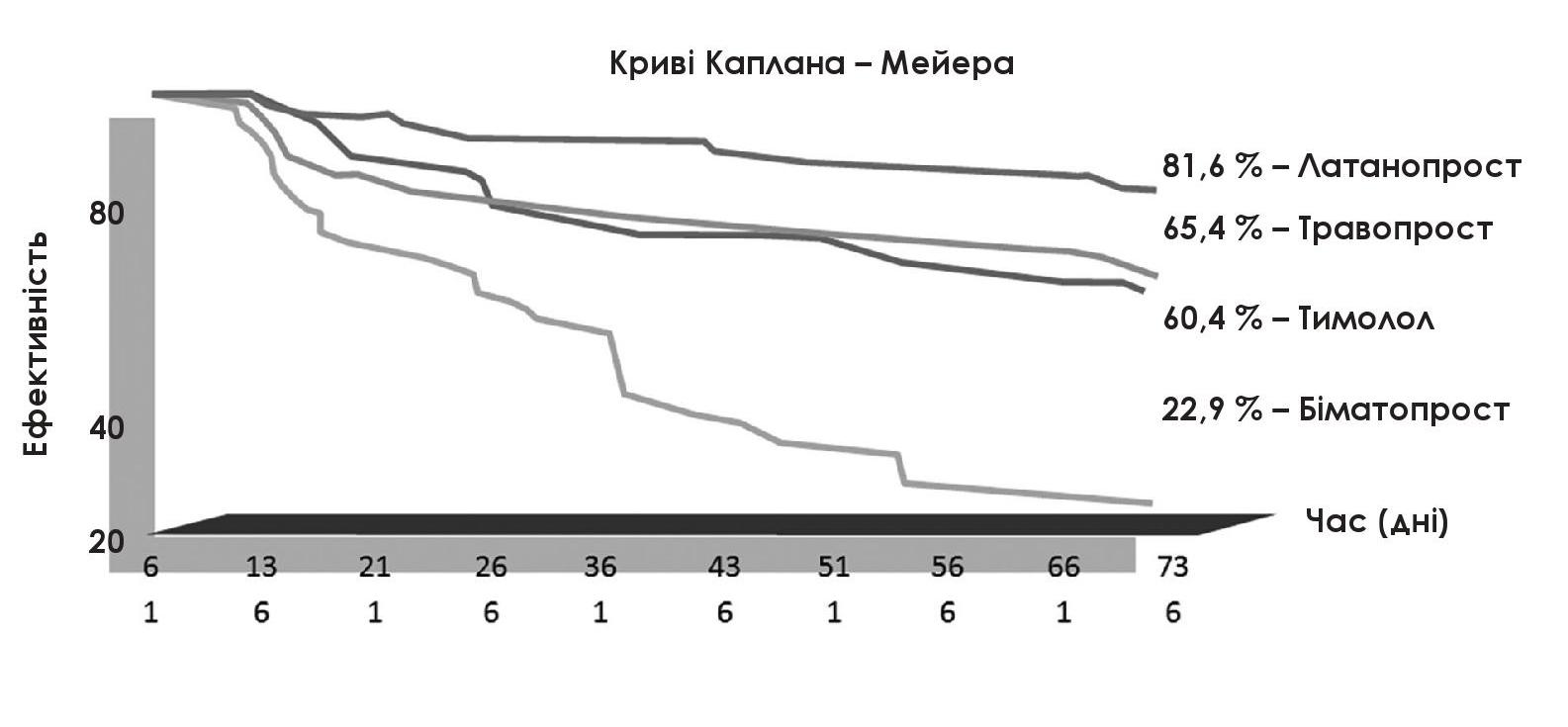
Рисунок 1. Гіпотензивна ефективність та % прихильних до терапії пацієнтів протягом 2 років спостереження
Відомо, що молекула латанопросту має високу ліпофільність, добре розчинна у жирах, легко проникає через рогівку в передню камеру ока завдяки спорідненим властивостям до клітинних мембран та «працює» в низькій концентрації. Це дозволяє призначати препарат у малих дозах для отримання бажаного гіпотензивного ефекту з відмінною переносимістю. Однак латанопрост погано розчиняється у воді, потребує додаткового вмісту емульгатора та стабілізатора, має достатню нестабільність згідно з інструкцією та вимагає зберігання в холодильнику [8, 9, 13, 14, 18, 21].
Цю проблему вирішували завдяки консервантам (бензалконія хлорид (БАХ)), які виконували три функції: 1) емульгацію простагландину; 2) стабілізацію в розчині; 3) антимікробну дію. Але БАХ зумовлює пошкодження очної поверхні, особливо при довготривалому використанні. БАХ індукує апоптоз, стимулює вироблення супероксиду та збільшує рівень запальних медіаторів, що призводить до зменшення кількості келихоподібних клітин, розриву міжклітинних з’єднань клітин рогівки, розриву слізної плівки та знищення епітеліального бар’єра рогівки, зниження сльозопродукції, спричиняє токсичний вплив на рогівку. БАХ також накопичується і справляє токсичний вплив на важливі в патогенезі глаукоми зони: епітеліальні клітини трабекули та сітківку в зоні зорового нерва та макули, що може погіршувати перебіг глаукоми [3, 4, 7, 10, 12].
Для БАХ характерний ефект кумуляції, тобто з часом він накопичується у тканині рогівки та кон’юнктиви, завдяки чому його негативний токсичний та прозапальний вплив збільшується. Це негативно впливає на стан поверхні ока та на перебіг глаукомного процесу за рахунок зменшення гіпотензивного ефекту антиглаукомних крапель [3, 4, 7, 10, 12, 15, 16].
Зважаючи на всі ці недоліки, на сьогодні позитивно заявив про себе антиглаукомний препарат Монопрост (латанопрост без вмісту консерванту в матриксі Протріаксину). Протріаксин поєднує в собі декілька полімерів, які добре переносяться, розчиняють і стабілізують простагландин, що призводить до відмінної стабільності при збереженні ефективності [3].
Підтвердженням ефективності є дослідження Руланда (2013), яке засвідчує, що Монопрост співставний за ефективністю з еталонним простагландином, але має кращий рівень переносимості, комфорту й менше подразнює поверхню ока [3, 4].
Мета – провести аналіз ефективності застосування препарату Монопрост у лікуванні пацієнтів з первинною відкритокутовою глаукомою порівняно з оригінальним препаратом латанопросту з консервантом.
Матеріали та методи
У групи дослідження входили 40 пацієнтів віком 65–75 років з ПВКГ та некомпенсованим ВОТ. Середній вік хворих становив 62,5 ± 7,1 року. Після включення пацієнти були рандомізовані для отримання зіставних груп за віком і рівнем вихідного офтальмотонусу. Група І (контрольна), до якої увійшло 20 пацієнтів (26 очей), отримувала оригінальний латанопрост з консервантом (Ксалатан) у вигляді одноразової інстиляції один раз на ніч. Група ІІ (основна) – 20 пацієнтів (26 очей) – отримувала препарат Монопрост так само у вигляді одноразової інстиляції один раз на ніч.
Гостроту зору оцінювали за допомогою візометрії стандартним методом з використанням проектора оптотипів і набору коригувальних скелець. Внутрішньоочний тиск вимірювали апаратом iCare-100, периметрію виконували на апараті Field Analyzer фірми Humphrey, оптичну когерентну томографію (ОКТ) – на обладнанні Huvitz HOCT-1F.
За результатами ОКТ визначали середню товщину шару нервових волокон сітківки (RNFL Thickness), параметри головки зорового нерва (об’єм нейроретинального пояска (rim volume)), об’єм головки зорового нерва (nerve head volume), об’єм екскавації (cup volume) і середню товщину шару гангліонарних клітин сітківки (GCC Thickness Average).
Загальний час дослідження становив 12 тижнів. Оцінювання ВОТ проводили на початку дослідження та через 2, 6, 12 тижнів, а зорових функцій та морфометрії сітківки також на початку і наприкінці дослідження, тобто через 12 тижнів від початку терапії.
Результати та обговорення
Рівні ВОТ в обох групах на етапі скринінгового дослідження були зіставлені за даними середніх величин офтальмотонусу: 26,4 ± 2,6 мм рт. ст. в контрольній групі І з оригінальним латанопростом з консервантом та 26,3 ± 2,7 мм рт. ст. – в основній групі з Монопростом. Через 2 тижні терапії в групі І середній показник Ро знизився на 30 % – до 18,6 ± 2,5 мм рт. ст. (p > 0,05), у II групі – на 31 % (до 18,2 ± 2,2 мм рт. ст., p > 0,05).
Через 6 тижнів інстиляційного режиму рівень Ро знизився відповідно на 31 та 34 %, тобто до 18,2 ± 2,8 та 17,4 ± 2,5 мм рт. ст. (р > 0,05), відповідно у групах I та II. До кінця терміну спостереження (тобто через 12 тижнів) зниження ВОТ від початкового рівня досягло 29 % і 32 % (відповідно до 18,7 ± 2,7 і 18,0 ± 2,5 мм рт. ст., p > 0,05) (таблиця 2).
Таблиця 2. Порівняльна динаміка показників ВОТ в І (контрольна) та ІІ (основна) групах

Отже, середнє зниження офтальмотонусу в обох групах становило близько 1/3 від початкового значення.
Динаміка функціональних показників
На кінцевому терміні спостереження (за 12 тижнів) в обох групах було відзначено поліпшення гостроти зору порівняно з вихідними даними: з 0,77 ± 0,1 до 0,82 ± 0,1 (на 6,5 %) у групі пацієнтів (група I), які отримували оригінальний латанопрост з консервантом (p > 0,05 ), і з 0,76 ± 0,1 до 0,83 ± 0,1 (на 9,2 %) (p < 0,05) у хворих, які використовували Монопрост (група II), що може бути пояснено гіпотензивною, тобто непрямою нейропротекторною дією очних крапель (таблиця 3).
Таблиця 3. Порівняння динаміки змін гостроти зору в І та ІІ групах (гострота зору)
Динаміка показників комп’ютерної периметрії
В обох групах за 12 тижнів було відзначено достовірне збільшення середньої величини стандартного відхилення MD: з –5,8 ± 2,7 до 5,3 ± 2,5 дБ в I групі (p < 0,05) і з –6,6 ± 2,0 до 5,9 ± 1,9 дБ – у II групі (p < 0,05). Середнє значення патерну стандартного відхилення (PSD) достовірно знизилося з 5,9 ± 2,0 до 5,4 ± 1,9 дБ (p < 0,05) і з 5,6 ± 1,9 до 5,0 ± 1,7 дБ (p < 0,05) відповідно. Достовірна позитивна динаміка периметральних індексів в обох групах до кінця терміну спостереження, на наш погляд, пояснюється реакцією гангліонарних клітин на істотне зниження офтальмотонусу, тобто ефектом непрямої нейропротекції (таблиця 4).
Таблиця 4. Порівняння динаміки периметричних індексів в І та ІІ групах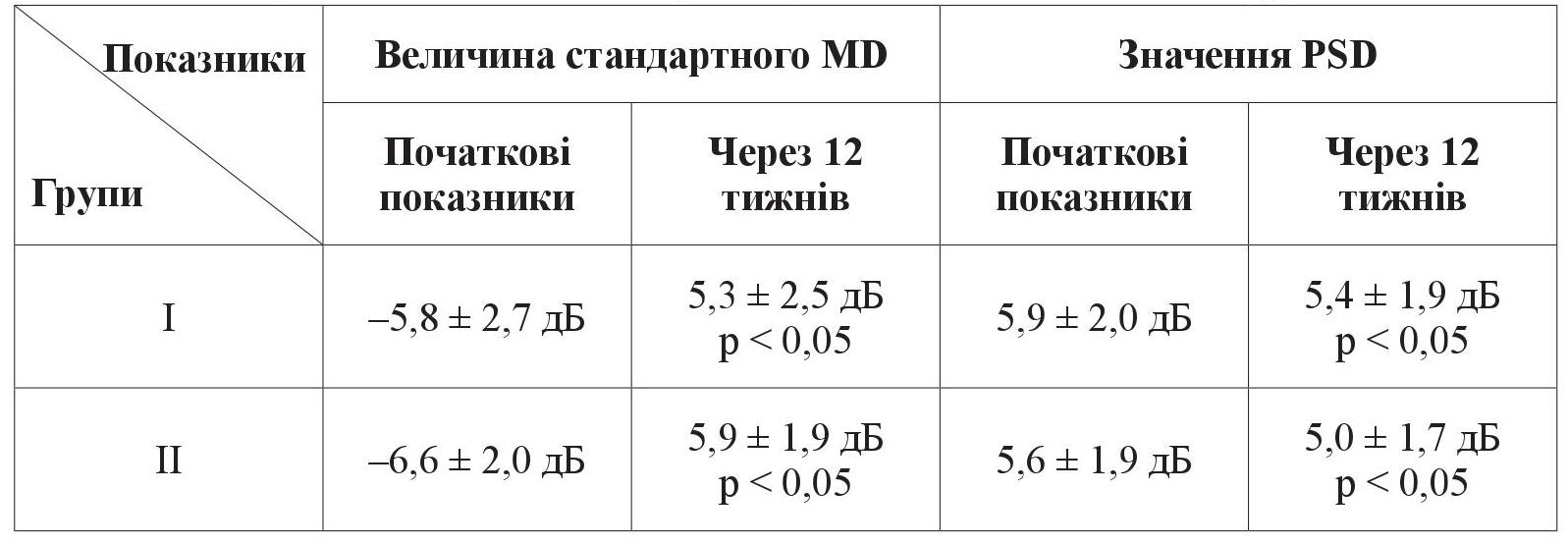
Динаміка показників ОКТ
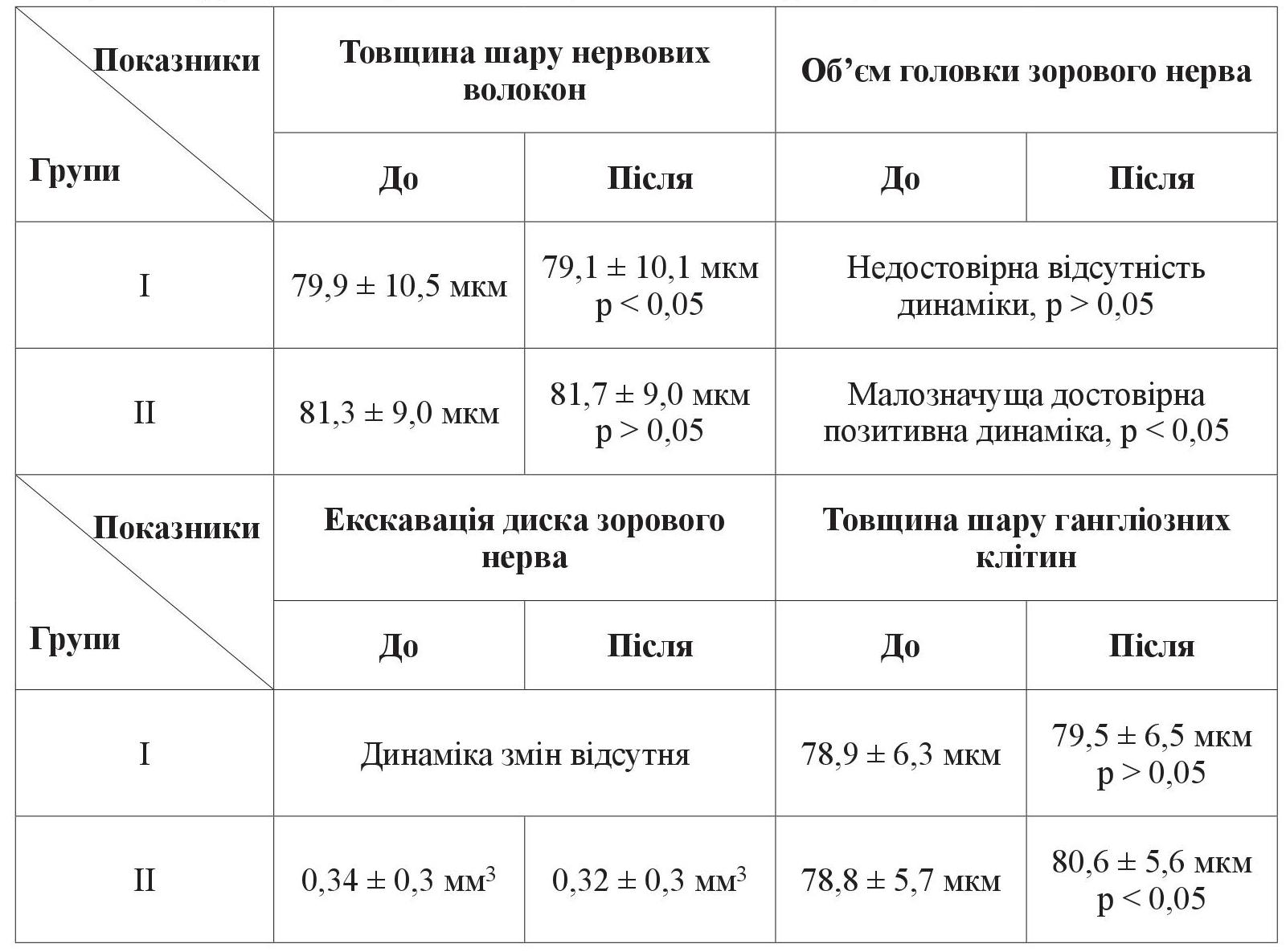
Через 12 тижнів у групі з оригінальним латанопростом з консервантом була відзначена достовірна слабко негативна динаміка показника середньої товщини шару нервових волокон сітківки: зменшення з 79,9 ± 10,5 до 79,1 ± 10,1 мкм (p < 0,05), у той час як у групі з Монопростом спостерігалася недостовірна слабко позитивна динаміка, тобто збільшення з 81,3 ± 9,0 до 81,7 ± 9,0 мкм (p > 0,05).
Недостовірна відсутність динаміки об’єму головки зорового нерва була зафіксована в I групі (p > 0,05), тоді як у II групі була відзначена малозначуща достовірна позитивна динаміка (p < 0,05).
Будь-яка динаміка величини об’єму екскавації диска зорового нерва в I групі була відсутня, у II групі, хоча і недостовірно, було зафіксовано її зменшення з 0,34 ± 0,3 до 0,32 ± 0,3 мм3.
В обох групах була зафіксована позитивна динаміка величини шару комплексу гангліонарних клітин сітківки: з 78,9 ± 6,3 до 79,5 ± 6,5 мкм у групі з оригінальним латанопростом з консервантом (p > 0,05) і з 78,8 ± 5, 7 до 80,6 ± 5,6 мкм – у групі з Монопростом (p < 0,05) (таблиця 5).
Таблиця 5. Порівняння динаміки показників ОКТ в І та ІІ групах (товщина шару нервових волокон,
об’єм головки зорового нерва, екскавація диска зорового нерва, товщина шару гангліонарних клітин) за 12 тижнів дослідження
Обговорення
Отримані дані свідчать про розширення можливості корекції ВОТ у хворих із ПВКГ завдяки появі безконсервантної форми латанопросту серед групи препаратів простагландинів. За даними 12-тижневого спостереження за хворими, що отримували лікування оригінальним латанопростом з консервантом та латанопростом без умісту консерванту (Монопрост), визначено високу гіпотензивну дію в середньому на рівні 31 %, що відповідає сучасним вимогам до зниження ВОТ з метою стабілізації зорових функцій. Препарат Монопрост продемонстрував високий рівень ефективності, безпеки та прихильності на основі аналізу даних комп’ютерної периметрії та ОКТ
Висновки
1. Гіпотензивний безконсервантний препарат Монопрост з групи аналогів простагландинів за даними 12-тижневого спостереження виявив достатній гіпотензивний ефект порівняно з гіпотензивною дією оригінального латанопросту: зниження ВОТ наприкінці дослідження становило 32 % на Монопрості та 29 % – на еталонному латанопрості з консервантом.
2. Гіпотензивна дія Монопросту та відсутність токсичного впливу консервантів призводять до ефекту непрямої нейропротекції та сприяють покращенню гостроти зору (на 9,2 %), а також позитивній динаміці змін функціональних показників за даними оптичної когерентної томографії та комп’ютерної периметрії з різним ступенем достовірності.
3. Препарат характеризується низьким рівнем місцевих побічних ефектів і може бути рекомендований для гіпотензивної терапії пацієнтів з ПВКГ.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
REFERENCES
- Європейське глаукомне товариство. Термінологія та настанова з глаукоми. 4-е видання. 2018. 196 с. European Glaucoma Society. Terminology and Guidelines for Glaucoma. 4th Edition. 2018. 196 p.
- Бездетко ПА. Нейропротекторная терапия открытоугольной глаукомы: взгляд эксперта. Здоров’я України. 2018 Липень;13–14(434–435):35–6. Bezditko PA. [Neuroprotective therapy for open-angle glaucoma: expert opinion]. Zdorovia Ukrainy. 2018 July;13–14(434–435):35–6. Russian.
- Дрожжина ГИ, Групчева К, Мужичук ЕП. Монопрост – инновации в терапии глаукомы. Здоров’я України. 2018 Липень; 13–14(434–435):50–1. Drozhzhina GI, Grupcheva K, Muzhichuk EP. [Monoprost – Innovations in Glaucoma Therapy]. Zdorovia Ukrainy. 2018 July;13–14(434–435):50–1. Russian
- Dry eye diseases 2017 TFOS DESII Report of the International Dry Eye Workshop.
- EMEA Public Statement on Antimicrobial Preservatives in Ophthalmic Preparations for Human Use. EMEA/622721/2009, London, 08 December 2009.
- Khawaja Ap, Crabb DP, Jansonius NM. The role of ocular perfusion pressure in glaucoma cannot be studied with multivariable regression analysis applied to surrogates. Invest Ophthalmol Vis Sci. 2013;54(7):4619–20.
- Report of the Management and Therapy Subcommittee of the International Dry Eye Workshop (2017).
- Sena DF, Lindsley K. Neuroprotection for treatment of glaucoma in adult. The Cochrane database of systematic reviews. 2013;2:CD006539.
- Boland MV, Ervin AM, Friedman DS, et al. Comparative effectiveness of treatments for open-angle glaucoma: a systematic review for the U.S. Preventive Services Task Force. Ann Inrern Med. 2013;158(4):271–9.
- Thygesen J. Glaucoma therapy: preservative-free for all? Clinical Ophthalmology. 2018; 12:707–17.
- Peters D, Bengtsson B, Heijl A. Factors associated with lifetime risk of open-angle glaucoma blindness. Acta Ophthalmol. 2014;92(5):421–5.
- Rouland JF, Traverso CE, Stalmans I, Fekih LE, Delval L, Renault D, Baudouin C. Efficacy and safety of preservative-free latanoprost eyedrops, compared with BAK-preserved latanoprost in patients with ocular hypertension or glaucoma. Br J Ophthalmol. 2013 Feb; 97(2):196–200.
- Cucherat M, Rouland JF. Relative efficacy and safety of preservative-free latanoprost (T2345) for the treatment of open-angle glaucoma and ocular hypertension. An adjusted indirect comparison meta-analysis. Acta Ophtalmologica. 2012;90(s249).
- Cucherat M, Stalmans I, Rouland JF. Relative efficacy and safety of preservative-free latanoprost (T2345) for the treatment of open-angle glaucoma and ocular hypertension: an adjusted Indirect comparison meta-analysis of randomized clinical trials. J Glaucoma. 2014 Jan;23(1):e69–75.
- Economou MA, Laukeland H, Grabska-Liberek I, Rouland JF. Long-term efficacy and safety of preserved and preservative-free prostaglandins eyedrops. Final results of the FREE Survey. WGC 2017.
- Martinez-de-la-Casa JM, Perez-Bartolome F, Urcelay E, et al. Tear cytokine profile of glaucoma patients treated with preservative-free or preserved latanoprost. Ocul Surf. 2017; 15(4):723–9.
- Van der Valk R, Webers CA, Schouten JS, Zeegers MP, Hendrikse F, Prins MH. Intraocular pressure-lowering effects of all commonly used glaucoma drugs: a meta-analysis of randomized clinical trials. Ophthalmology. 2005;112(7):1177–85.
- Arias A, Schargel K, Ussa F, Canut MI, Robles AY, Sánchez BM. Patient persistence with first-line antiglaucomatous monotherapy. Clin Ophthalmol. 2010;4:261–7.
- Newman-Casey PA, Blachley T, Lee PP, Heisler M, Farris KB, Stein JD. Patterns of Glaucoma Medication Adherence over Four Years of Follow-Up. Ophthalmology. 2015; 122(10):2010–21.
- Lemij HG, Hoevenaars JG, van der Windt C, Baudouin C. Patient satisfaction with glaucoma therapy: reality or myth? Clin Ophthalmol. 2015;9:785–93.
- Aptel F, Choudhry R, Stalmans I. Preservative-free versus preserved latanoprost eye drops in patients with open-angle glaucoma or ocular hypertension. Curr Med Res Opin. 2016; 32(8):1457–63.
- Zheng Y Wong TY Mitchell P Distribution of ocular perfusion pressure and its relationship with open-angle glaucoma: the Singapore Malay Eye Study. Invest Ophthalmol Vis Sci. 2010;51:3399–404.
- Ramdas WD, Wolfs RC, Hofman A, et al. Ocular perfusion pressure and the incidence of glaucoma: real effect or artifact? The Rotterdam Study. Invest Ophthalmol Vis Sci. 2011; 52: 6875–81.
Стаття надійшла в редакцію 11.10.2019 р.
Рецензія на статтю надійшла в редакцію 25.10.2019 р.