- Автор: Super User
- Категорія: Український журнал «Офтальмологія» № 1 (11) 2020
- Опубліковано: 09 грудня 2020
- Перегляди: 3652
https://doi.org/10.30702/Ophthalmology30092020-11.1.2166-77
УДК 617.711-004.1
Веселовская З. Ф., профессор, член-корреспондент НАМН Украины
Веселовская Н. Н., профессор
Запорожченко И. Б., доцент
Киевский медицинский университет, Глазная клиника КНП «КМКЛ № 1», г. Киев, Украина
Резюме. В данном исследовании изучено влияние препаратов СуперОптикTM Аква и СуперОптикTM Комплит на состояние передней поверхности глаза в до- и послеоперационном периоде у пациентов с факоэмульсификацией (ФЭК) катаракты.
Материалы и методы. В исследование было включено 28 пациентов (56 глаз) в возрасте 59–80 лет. В первой группе пациентов с синдромом сухого глаза (ССГ) 1–2 ст. (а – 14 глаз; b – 14 глаз) за 2 недели до ФЭК и в послеоперационном периоде был использован препарат СуперОптикTM Аква по 1 капле 2–3 раза в день. Во второй группе пациентов с ССГ 3–4 ст. (с – 14 глаз, d – 14 глаз) за 2 недели до ФЭК и в послеоперационном периоде был использован препарат СуперОптикTM Комплит по 1 капле 2–3 раза в день.
Результаты. В данном исследовании показано, что улучшение качества жизни пациентов с ФЭК катаракты возможно при профилактике и терапии ССГ с помощью препаратов СуперОптикTM Аква и СуперОптикTM Комплит в зависимости от стадии ССГ.
Ключевые слова: факоэмульсификация, синдром сухого глаза.
Veselovska Z. F., Veselovska N. M., Zaporozhchenko I. B.
Kyiv Medical University, Eye Clinic of Kyiv City Hospital No 1, Kyiv, Ukraine
Possibility of Protection of the Anterior Surface of the Eye in Patients with Dry Eye Syndrome and Cataract
Abstract. The work is dedicated to investigation of influence of medications SuperOpticTM Aqua and SuperOpticTM Complit on to the anterior eye surface in before and postoperation period in patients with phaco.
Materials and methods. 28 patients (56 eyes) in age 59-80 were examined. In first group – patients with dry eye syndrome 1-2 st. (a, b: a – 14 eyes; b – 14 eyes) 2 weeks before the phaco and in postoperation period used SuperOpticTM Aqua in regimen 1 drop 2-3 times/day. In second group – patients with dry eye syndrome 3-4 st. (c – 14 eyes; d – 14 eyes) 2 weeks before the phaco and in postoperation period used SuperOpticTM Complit in regimen 1 drop 2-3 times/day.
Results. In this investigation we revealed improvement the quality of life in patients in prevention and treatment dry eye syndrome who undergone phaco with help of SuperOpticTM Aqua and SuperOpticTM Complit depending of the stage of dry eye syndrome.
Keywords: phacoemulsification, dry eye syndrome.
Проблема синдрома сухого глаза (ССГ) на сегодняшний день приобретает все большую актуальность в офтальмологической практике [3, 6, 7, 9, 11, 14, 19, 25], так как ССГ выявляют у 9–18 % людей, а среди пациентов офтальмологического профиля этот показатель достигает 45 % [11, 16, 20]. В течение последних 30 лет частота выявления ССГ увеличилась в 4,5 раза и это связано с внедрением в современную жизнь IT-технологий, смартфонов, компьютерных мониторных систем, кондиционеров, а также ухудшением экологической ситуации [16].
Согласно определению DEWSII 2017 года [9, 16, 18, 26], ССГ представляет собой заболевание глазной поверхности, с большим количеством факторов риска, которое характеризуется нарушением гомеостаза слезной пленки. Это сопровождается офтальмологическими симптомами – зудом, ощущением жжения, раздражением глаз, их покраснением, чувством наличия инородного тела, сухостью, расплывчатым зрением, восстанавливающимся после моргания, слезотечением, дискомфортом, который усиливается после зрительной работы, что приводит к снижению зрительной и общей работоспособности [4]. В развитии этих симптомов этиологическую роль играют нaрушение стабильности, гиперосмолярность слезной пленки, воспаление и повреждение глазной поверхности, а также нейросенсорные изменения [6, 9, 12, 13, 17, 27].
В современных условиях на сегодняшний день удаление катаракты является одной из наиболее распространенных и успешных хирургических операций [8]. Согласно проспективному мультицентровому исследованию P.H.A.C.O., проведенному William B. Trattler et al. в 2017 году, клинические признаки ССГ у пациентов с катарактой встречаются достаточно часто [5]. При этом многие пациенты (63,2 %) жалоб не предъявляют [9]. Пациенту в до- и послеоперационном периоде назначаются препараты, оказывающие негативное влияние на поверхность глаза или содержащие агрессивные консерванты [1, 14, 15, 21, 22].
При ведении данной группы пациентов задачей офтальмолога является выявление заболевания, своевременное направление на оперативное лечение, подготовка к операции, послеоперационное наблюдение. Для того чтобы операция и период восстановления прошли продуктивно, очень важно выявить состояния, негативно влияющие на конечный результат и удовлетворенность пациента [5, 17, 23, 28]. У пациентов с предшествующим ССГ это приводит к нарастанию его симптоматики, которая усиливает дискомфорт после операции. Такие пациенты часто посещают офтальмолога и жалуются на состояние своих глаз, высказывая неудовлетворенность результатами операции, несмотря на хороший послеоперационный результат [3, 10, 24].
Цель исследования
1. Изучение и клиническая оценка влияния препаратов СуперОптикTM Аква и СуперОптикTM Комплит на состояние передней поверхности глаза у пациентов с факоэмульсификацией (ФЭК) катаракты.
2. Оценка эффективности и безопасности лечения ССГ в пред- и послеоперационном периоде препаратами СуперОптикTM Аква и СуперОптикTM Комплит.
Материалы и методы
В исследование было включено 28 пациентов (56 глаз) в возрасте 59–80 лет. Среди пациентов было 14 (50 %) мужчин и 14 (50 %) женщин. Пациенты были разделены на 2 группы и 4 подгруппы (a – 1 ст., b – 2 ст., c – 3 ст., d – 4 ст.) (таблица 1) [2].
В 1-й группе пациентов с ССГ 1–2 ст. (подгруппы а (1), b (2) а – 14 глаз; b – 14 глаз) за 2 недели до ФЭК и в послеоперационном периоде был использован препарат СуперОптикTM Аква по 1 капле 2–3 раза в день. Во второй группе пациентов с ССГ 3–4 ст. (подгруппы с (3), d (4); с – 14 глаз, d – 14 глаз) за 2 недели до ФЭК и в послеоперационном периоде был использован препарат СуперОптикTM Комплит по 1 капле 3–4 раза в день. За 3 дня до операции обе группы пациентов местно согласно стандартной схеме получали антибиотик и нестероидные противовоспалительные препараты (НПВП). Пациенты наблюдались на протяжении 1 года.
Таблица 1. Классификация ССГ по тяжести симптомов
| Симптомы | Степень тяжести ССГ | ||||||
|---|---|---|---|---|---|---|---|
| Дискомфорт (тяжесть и частота) | 1 | 2 | 3 | 4 | |||
| Легкий, эпизодический (неблагоприятные факторы среды) | Средний, эпизодический или хронический (может возникать независимо от действия неблагоприятных факторов среды) | Тяжелый, частый или постоянный (независимо от действия факторов окружающей среды) | Тяжелый, постоянный, значительно затрудняющий жизнедеятельность | ||||
| Зрительные симптомы | Нет или эпизодическая легкая усталость | Эпизодические, легкие, ограничивающие деятельность | Хронические и постоянные, ограничивающие деятельность | Постоянные и значительно ограничивающие деятельность | |||
| Инъекция конъюнктивы | Нет или легкая | Нет или легкая | +/– | +/++ | |||
| Прокрашивание конъюнктивы | Нет или легкая | Непостоянное | От умеренного до выраженного | Выраженное | |||
| Тяжесть прокрашивания роговицы | Нет или легкое | Непостоянное | Выраженное в центральной зоне | Глубокие точечные эрозии | |||
| Время разрыва слезной пленки | Непостоянное | ≤ 10 с | ≤ 5 с | Незамедлительно | |||
| Проба Ширмера | Непостоянная | ≤ 10 мм / 5 мин | ≤ 5 мм / 5 мин | ≤ 2 мм / 5 мин | |||
В таблицах 2, 3 представлен состав глазных капель СуперОптикTM Аква и СуперОптикTM Комплит. СуперОптикTM Аква – препарат, содержащий натрия гиалуронат (0,1 %) и консервант полигексадин 20 % с бактерицидным эффектом. В состав препарата СуперОптикTM Комплит входит натрия гиалуронат (0,2 %).
Таблица 2. СуперОптикTM Аква
| Молекула | Количество | Значение |
|---|---|---|
| Натрия гиалуронат (тяжелая полимерная молекула – 800–1200 кДа) | 1 мг (0,1 %) | Лубрикант – смазывает поверхность глаза, притягивает воду |
| Борная кислота | 6 мг (0,6 %) | Буфера – создают рН, который приближен к физиологичному (6,6–7,8) |
| Натрия тетраборат гидратированный | 0,663 мг (0,06 %) | |
| Натрия хлорид | 5,5 мг (0,5 %) | Осмотический эффект |
| Динатрия эденат | 0,5 мг (0,05 %) | Стабилизирует раствор и усиливает действие консерванта |
| Раствор полигексадина | 20 % | Консервант с бактерицидным эффектом |
Таблица 3. СуперОптикTM Комплит
| Молекула | Количество | Значение |
|---|---|---|
| Натрия гиалуронат (тяжелая полимерная молекула – 800–1200 кДа) | 2 мг (0,2 %) | Лубрикант – смазывает поверхность глаза, притягивает воду |
| Декспантенол | 2 мг (0,2 %) | Репаративный и противовоспалительный эффект |
| Натрия цитрат, дигидрат, кислота лимонная моногидрат | 0,663 мг (0,06 %) | Буфера – создают рН, который приближен к физиологичному (6,6–7,8) |
Всем пациентам 1-й и 2-й групп было выполнено стандартное офтальмологическое обследование перед операцией, включающее визометрию стандартным методом с использованием оптотипов и набора корригирующих стекол, биомикроскопию, офтальмоскопию, тонометрию (Icare-100), пахиметрию (OCT Visante, Zeiss), статистическую периметрию (Field Analyzer, Humphrey). С целью выявления типичных для ССГ жалоб был использован стандартизированный тест-опросник («индекс поражения поверхности глаза») [7, 26], проведены тест Ширмера, проба Норна, определение времени разрыва слезной пленки. Тест-опросник позволил в дальнейшем оценить переносимость пациентами проводимой терапии (таблица 4). Согласно результатам тест-опросника cредний коэффициент анкетирования OSDI перед началом лечения составлял: 1а – 21,25 ± 3,75; 1b – 30,21 ± 5,21; 2c – 55,48 ± 5,62; 2d – 95,45 ± 4,55.
Таблица 4. Оценка стадии ССГ в зависимости от выраженности симптомов согласно результатам анкеты OCULAR SURFACE DISEASE INDEX© (OSDI©)
| Группа пациентов | Стадия ССГ | Количество пациентов | Сумма балов (D) | Количество отвеченных вопросов | Коэффициент анкетирования |
|---|---|---|---|---|---|
| 1a | I | 2 | 12 | 12 | 25,0 |
| 3 | 10 | 12 | 20,83 | ||
| 2 | 10 | 11 | 22,72 | ||
| 3 | 9 | 11 | 20,45 | ||
| 4 | 7 | 10 | 17,5 | ||
| 1b | II | 1 | 17 | 12 | 35,42 |
| 1 | 15 | 12 | 31,25 | ||
| 1 | 15 | 11 | 34,04 | ||
| 3 | 14 | 10 | 35,0 | ||
| 2 | 13 | 10 | 32,5 | ||
| 5 | 9 | 9 | 25,0 | ||
| 1 | 9 | 8 | 28,12 | ||
| 2c | III | 4 | 27 | 12 | 56,25 |
| 2 | 22 | 11 | 50,0 | ||
| 3 | 22 | 9 | 61,1 | ||
| 1 | 18 | 9 | 49,86 | ||
| 1 | 19 | 8 | 59,37 | ||
| 3 | 15 | 7 | 53,57 | ||
| 2d | IV | 2 | 45 | 12 | 93,75 |
| 3 | 40 | 11 | 90,9 | ||
| 3 | 43 | 10 | 100,0 | ||
| 2 | 42 | 9 | 100,0 | ||
| 2 | 30 | 8 | 93,75 | ||
| 1 | 38 | 7 | 100,0 | ||
| 1 | 41 | 7 | 100,0 |
Основными жалобами у пациентов 1-й и 2-й групп были сухость, гиперемия, зуд век, дискомфорт в глазах. Субъективные жалобы пациентов 1-й и 2-й групп на протяжении 12 месяцев представлены в таблицах 5, 6.
Таблица 5. Динамика субъективных жалоб пациентов 1-й группы
| Сроки наблюдения, месяцы | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Жалобы | До лечения | 1 неделя | 1 месяц | 3 месяца | 6 месяцев | 12 месяцев | ||||||
| a | b | a | b | a | b | a | b | a | b | a | b | |
| Сухость | 12 | 12 | 8 | 9 | 6 | 7 | 4 | 5 | 1 | 2 | 0 | 1 |
| Гиперемия | 1 | 2 | 1 | 2 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Зуд век | 9 | 10 | 8 | 9 | 5 | 6 | 2 | 3 | 0 | 1 | 0 | 0 |
| Дискомфорт в глазах | 14 | 14 | 9 | 11 | 7 | 9 | 5 | 8 | 3 | 4 | 1 | 2 |
Таблица 6. Динамика субъективных жалоб пациентов 2-й группы
| Сроки наблюдения, месяцы | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Жалобы | До лечения | 1 неделя | 1 месяц | 3 месяца | 6 месяцев | 12 месяцев | ||||||
| c | d | c | d | c | d | c | d | c | d | c | d | |
| Сухость | 14 | 14 | 9 | 10 | 7 | 8 | 5 | 6 | 3 | 4 | 1 | 2 |
| Гиперемия | 14 | 14 | 12 | 13 | 11 | 12 | 8 | 9 | 6 | 5 | 0 | 1 |
| Зуд век | 13 | 13 | 10 | 11 | 9 | 10 | 7 | 8 | 2 | 3 | 1 | 1 |
| Дискомфорт в глазах | 11 | 12 | 10 | 11 | 9 | 10 | 5 | 6 | 3 | 4 | 1 | 2 |
Результаты
Анализ проведенного исследования показал, что признаки нестабильности слезной пленки и симптомы дискомфорта отмечались у всех пациентов (таблицы 7, 8).
Принимая во внимание результаты тест-опросника, функциональных тестов и учитывая степень тяжести ССГ, был выбран препарат, содержащий гиалуроновую кислоту: для 1-й группы – 0,1 % СуперОптикTM Аква, для 2-й группы – 0,2 % СуперОптикTM Комплит.
Динамика времени разрыва слезной пленки у пациентов 1-й и 2-й групп представлена на рисунке 1.
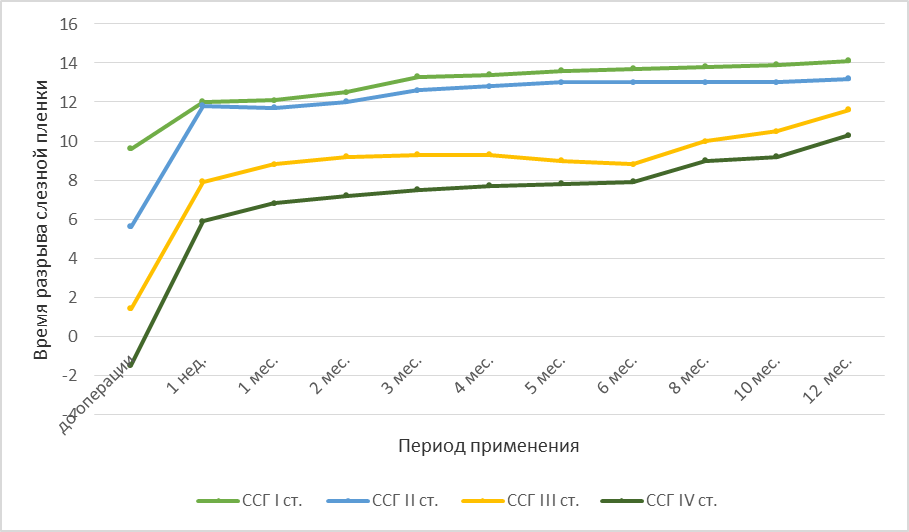
Рисунок 1. Время разрыва слезной пленки у пациентов 1-й и 2-й групп в разные сроки: по оси абсцисс – время лечения (месяцы); по оси ординат – показатели времени разрыва слезной пленки
Таблица 7. Динамика результатов исследований у пациентов 1-й группы
| Сроки наблюдения, месяцы | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Результаты исследований | До лечения | 2 недели | 1 месяц | 3 месяца | 6 месяцев | 12 месяцев | ||||||
| a | b | a | b | a | b | a | b | a | b | a | b | |
| Тест Ширмера, мм | 10,9 ± 0,4 | 8,2 ± 0,7 | 11,3 ± 0,3 | 8,9 ± 0,6 | 11,4 ± 0,1 | 9,7 ± 0,4 | 11,3 ± 0,2 | 10,0 ± 0,2 | 11,6 ± 0,3 | 10,2 ± 0,1 | 11,9 ± 0,2 | 10,5 ± 0,3 |
| Проба Норна, с | 9,8 ± 0,4 | 8,5 ± 0,3 | 10,2 ± 0,3 | 8,9 ± 0,5 | 10,4 ± 0,4 | 9,6 ± 0,6 | 10,6 ± 0,8 | 9,9 ± 0,4 | 10,6 ± 0,5 | 9,9 ± 0,3 | 10,7 ± 0,5 | 10,3 ± 0,4 |
| Время разрыва слезной пленки, с | 9,7 ± 0,7 | 7,5 ± 1,1 | 12 ± 0,6 | 11,8 ± 0,8 | 12,1 ± 0,5 | 12 ± 0,4 | 13,3 ± 0,4 | 12,6 ± 0,5 | 13,7 ± 0,2 | 13 ± 0,4 | 14,1 ± 0,1 | 13,2 ± 0,1 |
| Коэффициент анкетирования OSDI | 21,25 ± 3,75 | 30,21 ± 5,21 | 19,78 ± 3,13 | 29,54 ± 27 | 17 ± 3,12 | 22,22 ± 2,78 | 16,66 ± 2,08 | 17,18 ± 1,56 | 12,49 ± 2,08 | 14,01 ± 2,51 | 8,69 ± 0,39 | 14,06 ± 1,56 |
Таблица 8. Динамика результатов исследований у пациентов 2-й группы
| Сроки наблюдения, месяцы | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Результаты исследований | До лечения | 2 недели | 1 месяц | 3 месяца | 6 месяцев | 12 месяцев | ||||||
| c | d | c | d | c | d | c | d | c | d | c | d | |
| Тест Ширмера, мм | 2,9 ± 0,4 | 0,7 ± 0,7 | 3,3 ± 0,3 | 1,4 ± 0,6 | 4,6 ± 0,1 | 2,7 ± 0,4 | 5,2 ± 0,2 | 3,8 ± 0,2 | 7,9 ± 0,3 | 5,8 ± 0,1 | 9,4 ± 0,2 | 8,1 ± 0,3 |
| Проба Норна, с | 4,4 ± 0,3 | 2,1 ± 0,2 | 4,7 ± 0,4 | 2,8 ± 0,5 | 5,6 ± 0,3 | 3,8 ± 0,4 | 7,0 ± 0,6 | 5,2 ± 0,5 | 8,1 ± 0,5 | 6,3 ± 0,4 | 8,3 ± 0,3 | 7,1 ± 0,2 |
| Время разрыва слезной пленки, с | 3,3 ± 0,3 | 0,4 ± 0,1 | 7,9 ± 0,5 | 5,9 ± 0,4 | 9,0 ± 0,5 | 6,9 ± 0,4 | 9,3 ± 0,6 | 7,5 ± 0,5 | 8,8 ± 0,3 | 7,9 ± 0,2 | 11,6 ± 0,4 | 10,3 ± 0,3 |
| Коэффициент анкетирования OSDI | 55,48 ± 5,62 | 95,45 ± 4,55 | 48,61 ± 6,94 | 61,1 ± 5,5 | 43,05 ± 4,16 | 47,22 ± 3,44 | 27,78 ± 2,78 | 37,5 ± 4,17 | 19,44 ± 2,77 | 28,57 ± 3,79 | 13,89 ± 2,78 | 24,88 ± 2,38 |
Результаты теста Ширмера (длина увлажненной части тест-полоски) до начала лечения составляли в 1а группе 10,9 ± 0,4; 1b – 8,2 ± 0,7; во 2с – 2,9 ± 0,4, во 2d – 0,7 ± 0,7. Результаты пробы Ширмера после 2 недель лечения в 1а – 11,3 ± 0,3; 1b – 8,9 ± 0,6; во 2с – 3,3 ± 0,3, во 2d – 1,4 ± 0,6. Через 1 месяц: в 1а – 11,4 ± 0,1; в 1b – 9,7 ± 0,4; во 2с – 4,6 ± 0,1, во 2d – 2,7 ± 0,4. Через 6 месяцев: в 1а – 11,6 ± 0,3; в 1b – 10,2 ± 0,1; во 2с – 7,9 ± 0,3, во 2d – 5,8 ± 0,1. Через 12 месяцев: в 1а – 11,9 ± 0,2; в 1b – 10,5 ± 0,3; во 2с – 9,4 ± 0,2 , во 2d – 8,1 ± 0,3. Наблюдалось улучшение теста Ширмера у пациентов 1-й и 2-й групп, что свидетельствовало о повышении слезопродукции и снижении воспалительного процесса.
Через 2 недели, 1, 3, 6 и 12 месяцев отмечалось достоверное улучшение пробы Норна, что указывало на повышение стабильности слезной пленки.
Показатель времени разрыва слезной пленки (ВРСП) в подгруппах уменьшался по мере нарастания тяжести ССГ. До начала лечения показатель ВРСП составлял в 1а 9,7 ± 0,7; в 1b – 7,5 ± 1,1; во 2с – 3,3 ± 0,3, во 2d – 0,4 ± 0,1. На фоне лечения отмечено увеличение времени разрыва слезной пленки во всех подгруппах. Через 2 недели показатель ВРСП составлял в 1а – 12 ± 0,6; в 1b – 11,8 ± 0,8; во 2с – 7,9 ± 0,5, во 2d – 5,9 ± 0,4. Через 1 месяц показатель ВРСП составлял в 1а – 12,1 ± 0,5; в 1b – 12 ± 0,4; во 2с – 9,0 ± 0,5, во 2d – 6,9 ± 0,4. Через 6 месяцев показатель ВРСП составлял в 1а – 13,7 ± 0,2; в 1b – 13 ± 0,4; во 2с – 8,8 ± 0,3, во 2d – 7,9 ± 0,2. Через 12 месяцев показатель ВРСП составлял в 1а –14,1 ± 0,1; в 1b – 13,2 ± 0,1; во 2с – 11,6 ± 0,4, во 2d – 10,3 ± 0,3.
В обеих группах отмечалось достоверное снижение коэффициента OSDI в процессе лечения на протяжении 12 месяцев наблюдения.
Выводы
1. Своевременная диагностика и адекватное лечение в пред- и послеоперационном периоде у пациентов с катарактой являются важной задачей для офтальмолога в ведении данной категории больных.
2. Оптимизировать течение послеоперационного периода, улучшить качество жизни пациентов, а также предотвратить осложнения возможно при профилактике и терапии ССГ с помощью препаратов СуперОптикTM Аква и СуперОптикTM Комплит в зависимости от стадии ССГ.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
REFERENCES
- Акулов СН, Бабиева МВ. Послеоперационное ведение пациентов после факоэмульсификации. Офтальмология. 2013;10(4):59-61. Akulov SN, Babieva MV. [Postoperative maintaining patients after a phacoemulsifcation]. Ophthalmology in Russia. 2013;10(4):59-61. Russian. https://doi.org/10.18008/1816-5095- 2013-4-59-61
- Анисимова СГ, Мазина НК, Абрамова ТВ. Современные классификация и фармакотерапия синдрома «Сухого глаза». Вятский медицинский вестник. 2016;4(52):4-11. Anisimova SG, Mazina NK, Abramova TV. [Modern Classification and Pharmacotherapy of «Dry Eye» Syndrome]. Vyatskiy meditsinskiy vestnik. 2016;4(52):4-11. Russian.
- Астахов СЮ, Ткаченко НВ. Эффективность трегалозы в лечении синдрома «Сухого глаза» после факоэмульсификации. Офтальмол. ведомости. 2016;9(4):79-89. Astakhov SYu, Tkachenko NV. [Trehalose Efficacy in Dry Eye Syndrome Treatment after Phacoemulsifcation]. Ophthalmology Journal. 2016;9(4):79-89. Russian. https://doi.org/10.17816/ OV9479-89
- Бай УА. Синдром сухого ока. Медсестринство. 2019;(2):74-5. Bai UA. [Dry Eye Syndrome]. Nursing. 2019;(2):74-5. Ukrainian. https://doi.org/10.11603/2411-1597.2019.2.10220
- Бржеский ВВ, Голубев СЮ. Синдром сухого глаза и катаракта; [дата обращения 09.09.2020]. Режим доступа: https://www.moiglaza.ru/hcp/pronews/sindrom-suhogo-glaza/ssg-i-katarakta/ Brzheskiy VV, Golubev SYu. [Dry eye syndrome and cataracts]; [cited 2020 Sept 09]. Available from: https://www.moiglaza.ru/hcp/pronews/sindrom-suhogo-glaza/ssg-i-katarakta/
- Горенков РВ, Рябцева АА, Агафонов БВ, Дадашева МН, Ковальчук НА. Синдром сухого глаза в общей врачебной практике. Эффективная фармакотерапия. 2019;15(33):30-6. Gorenkov RV, Ryabtseva AA, Agafonov BV, Dadasheva MN, Kovalchuk NA. [Dry Eye Syndrome in General Medical Practice]. Effective Pharmacotherapy. 2019;15(33):30-6. Russian. https://doi.org/10.33978/2307-3586-2019-15-33-30-36
- Останина ДА, Коробинцева КН. Распpостраненность синдрома сухого глаза среди лиц молодого возраста. Вестник совета молодых учёных и специалистов Челябинской области. 2018;1(1 (20)):38-41. Ostanina DA., Korobinceva KN. [Prevalence of Dry Eye Syndrome among Young Persons]. Vestnik soveta molodykh uchenykh i spetsialistov Chelyabinskoy oblasti. 2018;1(1 (20)):38-41. Russian.
- Пирогов ЮИ, Бутина ГМ, Оксентюк АА, Хромова ЕС. Анализ результатов лечения пациентов с синдромом «Сухого глаза» бесконсервантными глазными каплями 0,3 % раствора гиалуроната натрия после факоэмульсификации. Офтальмол. ведомости. 2017; 10(2):73-7. Pirogov YuI, Butina GM, Oksentyuk AA, Khromova ES. [Analysis of Treatment Results In Dry Eye Syndrome Patients after Phacoemulsifcation by Preservative-Free 0.3% Sodium Hyaluronate Eye Drops]. Ophthalmology Journal. 2017;10(2):73-7. https://doi.org/10.17816/ OV10273-77
- Рыков СА, Дрожжина ГИ, Завгородняя НГ и др. Сухой глаз: последние новости в определении, классификации, диагностике и лечении. Здоров’я України. 2018;10(431):32-5. Rykov SA, Drozhzhina GI, Zavgorodnyaya NG et al. [Dry eye: the latest news in the definition, classification, diagnosis and treatment]. Zdorovia Ukrainy. 2018;10(431):32-5. Russian.
- Сахнов СН, Янченко СВ, Малышев АВ, Дашина ВВ, Цеева АР, Петросян ЛМ. Эпидемиология синдрома «сухого глаза» у пациентов перед хирургией катаракты. Офтальмология. 2020;17(2):281-9. Sakhnov SN, Yanchenko SV, Malyshev AV, Dashina VV, Ceeva AR, Petrosyan LM. [Dry Eye Epidemiology in Patients before Cataract Surgery]. Ophthalmology in Russia. 2020;17(2): 281-9. Russian. https://doi.org/10.18008/1816-5095-2020-2-281-289
- Седелкова ВА, Когай ВВ, Крайняя АС. Персонализированный подход в изучении синдрома «сухого глаза». Вестник совета молодых учёных и специалистов Челябинской области. 2018;2(3(22)):52-4. Sedelkova VA, Kogay VV, Krainyaya AS. [Personalized Approach in the Study of the Dry Eye Disease]. Vestnik soveta molodykh uchenykh i spetsialistov Chelyabinskoy oblasti. 2018; 2(3(22)):52-4. Russian.
- Современные представления о сухости глаза. Вестник оптометрии. 2018;2:45-8. [Modern ideas of dry eye]. Vestnik optometrii. 2018;2:45-8. Russian.
- Трубилин ВН, Полунина ЕГ, Анджелова ДВ, Куренков ВВ, Капкова СГ, Чиненова КВ, Коновалов МЕ, Пожарицкий МД. Современные представления об этиологии синдрома сухого глаза. Офтальмология. 2019;16(2):236-43. Trubilin VN, Polunina EG, Angelova DV, Kurenkov VV, Kapkova SG, Chinenova KV, Konovalov ME, Pozharitsky MD. [Current Concepts about the Etiology of Dry Eye Syndrome]. Ophthalmology in Russia. 2019;16(2):236-43. Russian. https://doi.org/10.18008/1816- 5095-2019-2-236-243
- Трубилин ВН, Седнева ТА, Капкова СГ. Слезозаместительная терапия в профилактике и лечении синдрома «сухого глаза» после катарактальной хирургии. Офтальмология. 2013;10(1):56-62. Trubilin VN, Sedneva TA, Kapkova SG. [The tear substitutive therapy for prophylaxis and treatment of dry eye after cataract surgery]. Ophthalmology in Russia. 2013;10(1):56-62.Russian. https://doi.org/10.18008/1816-5095-2013-1-56-62
- Уражанова МБ. Синдром «сухого глаза» в артифакичных глазах (обзор). Вестник АГИУВ. 2018;2:6-12. Urazhanova MB. [Syndrome of «Dry Eye» in Artifacical Eyes (Review)]. Herald ASIAME. 2018;2:6-12. Russian.
- Чистик T. Синдром сухого глаза: cовременные возможности комплексной диагностики «Dedicated Dry Eye Clinic». Архів офтальмології України. 2019;7(3):74-80. Chistik T. [Dry eye syndrome: the modern capabilities of the comprehensive diagnosis of Dedicated dry eye clinic]. Arkhiv oftalmologii Ukrainy. 2019;7(3):74-80. Russian.
- Caceres V. Primer for dry eye diagnosis and treatment before dry eye. Eye World (AsiaPacific). 2017;13(2):55-7.
- Golden MI, Meyer JJ, Patel BC. Dry Eye Syndrome. In: StatPearls. Treasure Island (FL): StatPearls Publishing; July 2, 2020.
- Heidari M, Noorizadeh F, Wu K, Inomata T, Mashaghi A. Dry Eye Disease: Emerging Approaches to Disease Analysis and Therapy. J Clin Med. 2019;8(9):1439. https://doi.org/10.3390/jcm8091439
- Inomata T, Iwagami M, Nakamura M, Shiang T, Yoshimura Y, Fujimoto K, et al. Characteristics and Risk Factors Associated With Diagnosed and Undiagnosed Symptomatic Dry Eye Using a Smartphone Application. JAMA Ophthalmol. 2019 Nov 27;138(1):58-68. https://doi.org/10.1001/jamaophthalmol.2019.4815
- Walsh K, Jones L. The use of preservatives in dry eye drops. Clin Ophthalmol. 2019 Aug 1;13:1409-25. https://doi.org/10.2147/OPTH.S211611
- Kaštelan S, Tomić M, Salopek-Rabatić J, Novak B. Diagnostic procedures and management of dry eye. Biomed Res Int. 2013;2013:309723. https://doi.org/10.1155/2013/309723
- Kato K, Miyake K, Hirano K, Kondo M. Management of Postoperative Inflammation and Dry Eye After Cataract Surgery. Cornea. 2019;38 (Suppl 1):S25-S33. https://doi.org/10.1097/ICO.0000000000002125
- Brennan K. Calculating for Success: IOLs in Difficult Eyes. Review of ophthalmology. 2017 Jan 10;34-40.
- Liang LY, Li J, Liu ZG. [Focusing on the functional dry eye]. Zhonghua Yan Ke Za Zhi. 2019 Dec 11;55(12):885-90. Chinese. https://doi.org/10.3760/cma.j.issn.0412-4081.2019.12.003
- Stapleton F, Alves M, Bunya VY, Jalbert I, Lekhanont K, Malet F, et al. TFOS DEWS II Epidemiology Report. Ocul Surf. 2017;15(3):334-65. https://doi.org/10.1016/j.jtos.2017.05.003
- Tsubota K, Yokoi N, Watanabe H, Dogru M, Kojima T, Yamada M, et al. A New Perspective on Dry Eye Classification: Proposal by the Asia Dry Eye Society. Eye Contact Lens. 2020;46 Suppl 1(1):S2-S13. https://doi.org/10.1097/ICL.0000000000000643
- Trattler WB, Majmudar PA, Donnenfeld ED, McDonald MB, Stonecipher KG, Goldberg DF. The Prospective Health Assessment of Cataract Patients’ Ocular Surface (PHACO) study: the effect of dry eye. Clin Ophthalmol. 2017 Aug 7;11:1423-30. https://doi.org/10.2147/OPTH.S120159
Стаття надійшла в редакцію 18.09.2020 р.
Рецензія на статтю надійшла в редакцію 25.09.2020 р