- Автор: Super User
- Категорія: № 2 (07) 2017
- Опубліковано: 18 квітня 2018
- Перегляди: 7663
УДК 617.7−073.178
Оганесян А. А., Минасян А. Г., Cейранян В. М., Акопян В. Е.
Кафедра офтальмологии, Национальный институт здравоохранения им. С. Х. Авдалбекяна МЗ РА; Офтальмологическая служба МЦ «Эребуни»; Диагностический центр «Оптомед» Канада-Армения, г. Ереван, Армения
Резюме. Глазные капли, содержащие 1 % N-ацетилкарнозина (Clarastill™, Bruschettini, Genoa, Italy), были протестированы у пациентов с диабетической ретинопатией в рандомизированном слепом плацебо-контролируемом клиническом исследовании. Результаты исследования показали, что N-ацетилкарнозин в течение 6 месяцев статистически значимо (по сравнению с плацебо) снижает тяжесть диабетической ретинопатии по шкале ETDRS и предотвращает дальнейшее развитие заболевания (p < 0,001). Раннее длительное применение глазных капель Clarastill™ рекомендуется для профилактики диабетической ретинопатии у пациентов с сахарным диабетом. Принимая во внимание антиоксидантные, цитопротекторные, увлажняющие, смазывающие свойства N-ацетилкарнозина, использование глазных капель Clarastill™ оправдано до и после лазерной коагуляции сетчатки, а также при расширенной диабетической ретинопатии для предотвращения полной слепоты.
Ключевые слова: диабет, ретинопатия, лечение, N-ацетилкарнозин, Кларастилл.
ВВЕДЕНИЕ
Диабетическая ретинопатия является частым и серьезным осложнением сахарного диабета [3, 19, 49, 51]. Это прогреcсирующее заболевание, проявляющееся поражением сосудов сетчатки, ее отеком и растущей потерей зрения [27, 28]. В процессе развития заболевания в сетчатке образуются мелкие хрупкие сосуды, которые легко разрываются с кровоизлияниями в сетчатку и стекловидное тело. Со временем кровоизлияния организуются в рубцовую ткань, которая может быть причиной отслойки сетчатки, повышения глазного давления и т. д., что может существенно ухудшить зрение. В далекозашедших стадиях, известных как «диабетический макулярный отек» и «пролиферативная ретинопатия», диабетическое поражение глаз может вызвать выраженную потерю зрения и полную слепоту [43, 44]. Диабетический макулярный отек может развиться в любой стадии диабетической ретинопатии. Практически у всех больных с сахарными диабетом 1-го типа после 20 лет болезни диагностируют диабетическую ретинопатию, 20–30 % из них − в развитой стадии. Больные с сахарным диабетом 2-го типа также подвержены развитию диабетической ретинопатии: через 10–15 лет болезни у более чем 75 % имеется диабетическая ретинопатия [53, 56]. Из-за неуклонного роста заболеваемости диабетом в настоящее время в развитых странах диабетическая ретинопатия стала одной из ведущих причин слепоты в возрасте 30–60 лет и переросла в серьезную медико-социальную проблему [40, 43, 49]. По данным ВОЗ в настоящее время диабетом страдают более 150 млн человек, а к 2025 г. это количество удвоится [40]. От 3 до 5 % населения земного шара страдает сахарным диабетом. Ежегодно регистрируется более 600 тыс. вновь выявленных случаев заболевания, и это количество неуклонно растет [40].
Соответственно увеличивается и число больных диабетической ретинопатией [43, 44]. Специфическое лечение диабетической ретинопатии вначале было ограничено разрушением эпифиза [41]. С 1970 г. этот подход был полностью замещен фотокоагуляцией [24, 25]. Были получены положительные результаты при применении ксенонового и аргонового лазеров в профилактике слепоты при пролиферативной ретинопатии и макулярном отеке [29, 45]. Лазерная коагуляция революционизировала лечение диабетической ретинопатии, уменьшив риск потери зрения более чем на 50 % и став наиболее распространенным методом лечения этого осложнения [24, 25, 29]. Целью лазерной коагуляции является проведение прижиганий сетчатки, чтобы уменьшить потребность сетчатки в кислороде, устранить ишемию, приостановить новообразование сосудов и т. п. Однако лазерная фотокоагуляция эффективна только при своевременном применении, требует повторений. В результате ее проведения возможна потеря части периферического зрения и, в меньшей мере, цветного и сумеречного зрения [24, 29, 45]. В зависимости от ситуации применяются и некоторые альтернативные методы лечения диабетической ретинопатии и ее осложнений. Например, при значительном кровоизлиянии в стекловидное тело проводится витрэктомия [40]; с целью уменьшения макулярного отека в стекловидное тело инъецируется триамцинолон [36] и другие глюкокортикоиды, например, флуоцинолон [39], что, однако, может осложниться развитием стероидных катаракты и глаукомы, эндофтальмита и т. д. [36, 40]. В последнее время при диабетической ретинопатии предложены С-пептид [54], блокаторы инсулиноподобного фактора роста IGF-1 (octreotide) [32, 33] и ингибиторы сосудистого эндотелиального фактора роста (vascular endothelial growth factor – VEGF), в частности Авастин (Avastin™), Макуген (Macugen™), Лусентис (Lucentis™) и др. [40, 43]. По С-пептиду и октреотиду данные пока что неубедительны, эффект более выражен относительно симптомов диабета, а не ретинопатии per se, что касается ингибиторов VEGF, то их интравитреальное введение сопряжено с риском развития отслойки сетчатки, отека роговицы, катаракты, глаукомы, кровотечения, эндофтальмита (первоначально Авастин был предложен для лечения метастатического колоректального рака и вызывал при назначении множество побочных реакций, начиная от желудочно-кишечных перфораций и заканчивая кровотечениями, внутриартериальными тромбозами, инсультом, инфарктом миокарда, сердечно-сосудистой недостаточностью) [40, 43, 47]. В качестве пероральных и парентеральных средств борьбы с диабетической ретинопатией предложено большое количество препаратов разной направленности действия: ингибиторы альдоредуктазы [42], антиоксиданты [37], блокаторы ангиотензинконвертирующего фермента [10, 23, 38], блокаторы ангиотензиновых рецепторов (кандесартан) [48], мексидол [2], тиклодипин [50], ингибиторы протеинкиназы [3], аналоги соматостатина [40], пептидные биорегуляторы [16, 17], карбохромен [47], доксиум [15], дицинон [3], танакан [1], токоферол [3], эйконол [11], аспирин [26, 47], антигистаминные средства [32], диквертин [5, 13, 14], ксантинол [6], дипиридамол [46], гепарин [7], вобензим [4, 8, 12], эмоксипин [9] и множество других средств [11, 15], которые, однако, не обладают достаточной эффективностью и мало влияют на естественное развитие диабетической ретинопатии [19, 40, 47]. Рекомендацией отчаяния является призыв к тщательному гликемическому контролю больных с сахарным диабетом [51–53], но диабетическая ретинопатия часто развивается на фоне сравнительно низких показателей глюкозы в крови и, кроме того, компенсация сахарного диабета по мере увеличения длительности заболевания все более теряет свое влияние на развитие диабетической ретинопатии [3, 29, 35].
Таким образом, лечение диабетической ретинопатии продолжает оставаться сложной, проблематичной и актуальной задачей, требующей дальнейшего поиска эффективных средств профилактики и лечения.
МАТЕРИАЛ И МЕТОДЫ
N-ацетилкарнозин был клинически испытан в виде 1 % раствора глазных капель Кларастилл производства Брусчеттини, Италия (Clarastill™, Bruschettini, Genoa, Italy).
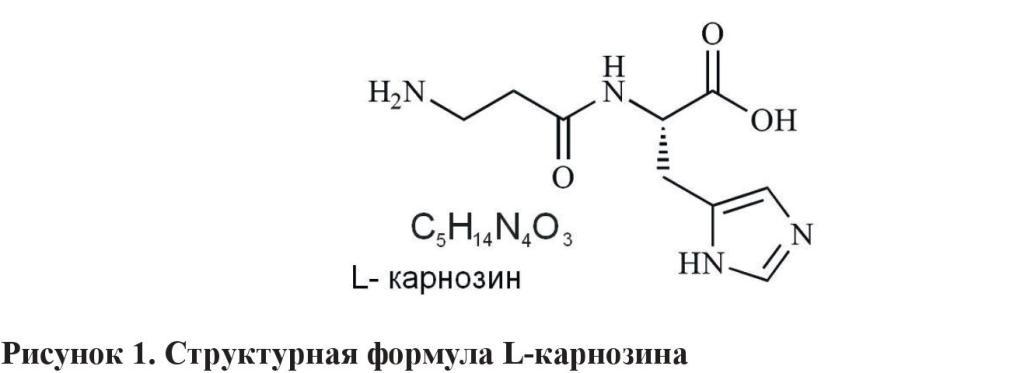
Основа N-ацетилкарнозина – L-карнозин (β-аланил-L-гистидин, C5H14N4O3, рисунок 1), был впервые обнаружен в начале прошлого века [35], открыв список регуляторных белков и пептидов – регуляторов метаболизма [20, 21]. N-ацетилкарнозин считается основным протективным фактором для тканей глаза и хорошо проходит через его тканевые барьеры [21, 22].
N-ацетилкарнозин является естественным физиологическим протективным дипептидом, синтезируемым в организме для защиты различных компонентов и тканей глаза от повреждения различными факторами внешней и внутренней среды и предотвращения дегенеративных процессов, связанных со старением как всего организма, так и тканей глаза в частности. Наибольшая концентрация N-ацетилкарнозина имеется в хрусталике и сетчатке глаз птиц, особенно дневных хищников, чья охота зависит от высокой остроты зрения на дальних дистанциях (орел, беркут, сокол и т. п.) [21, 22]. В отличие от птиц – ночных хищников (сова, филин и др.), у которых днем зрачки сужены («вертикальный зрачок») и защищают хрусталик и сетчатку от УФ-облучения и избыточного света, зрачки этих дневных хищников широко раскрыты, обеспечивая широкий доступ света и ультрафиолета на сетчатку. Стратегия охоты этих птиц влючает также зрение в диапазоне УФ-лучей, в частности регистрация УФ флуоресценции мочи грызунов и других мелких и более крупных животных обеспечивает им более успешное распознавание и охоту. N-ацетилкарнозин является тем протективным пептидом, который предохраняет хрусталик птиц от помутнения, а сетчатку глаза – от УФ ожога и дегенерации. Даже у наиболее долгоживущих птиц (орел, сокол, грифы, ворона и т. п.) благодаря N-ацетилкарнозину сохраняется прозрачность хрусталика, безукоризненное функционирование сетчатки и никогда не развиваются катаракта и патологические (включая возрастные) поражения сетчатки [22]. Экспериментально доказано, что N-ацетилкарнозин является исключительно выраженным антиоксидантным, цитопротективным, трофическим и гидратирующим натуральным пептидом [21, 22]. При этом не установлено каких-либо ограничений и противопоказаний к применению N-ацетилкарнозина и дипептид практически не проявляет токсичности даже при применении в крайне больших дозах.
Эффективность глазных капель определялась в условиях рандомизированного слепого плацебо-контролируемого испытания. Больных, по возможности, подбирали по принципу релевантности переменных.
Испытание было проведено у 148 больных (лечебная группа – 88 человек, контрольная – 60 человек), однако из-за разных причин (необходимость проведения фотокоагуляции из-за прогрессивного ухудшения зрения, прекращение закапывания капель, декомпенсация диабета, неявка на контрольные обследования и т. д.) к 6-месячной итоговой точке исследования пришли 114 больных (83 – из лечебной группы, 31 – из контрольной группы); не закончили клиническое испытание 29 человек из контрольной группы (15 были вынуждены прибегнуть к лазерной фотокоагуляции) и 5 – из группы лечения. Больные, включенные в клиническое испытание, страдали выраженной непролиферативной диабетической ретинопатией и ранней (невысокого риска) пролиферативной диабетической ретинопатией.
Лечебная группа получала глазные капли Кларастилл, содержащие 1 % N-ацетилкарнозин (1–2 капли два раза в день), контрольная группа – мягчительные глазные капли (1–2 капли два раза в день), не обладающие фармакологическим эффектом.
Больные, завершившие 6-месячное клиническое испытание, по возрасту, полу, длительности заболевания распределялись следующим образом: 1) лечебная группа (Кларастилл): возраст 31–55 лет – 9 больных, 14 глаз (5 мужчин, 4 женщины); 56–74 года – 58 больных, 106 глаз (31 мужчина, 27 женщин); 75 лет и более – 16 больных, 31 глаз (5 мужчин, 11 женщин), всего – 83 больных, 151 глаз (41 мужчина, 42 женщины); длительность заболевания: до 5 лет – 2 больных, 2 глаза; 5–9 лет – 14 больных, 23 глаза; 10–14 лет – 34 больных; 64 глаза; 15–19 лет – 28 больных, 53 глаза; более 20 лет – 5 больных, 9 глаз; 2) контрольная группа: возраст 31–55 лет – 6 больных, 10 глаз (3 мужчины, 3 женщины); 56–74 года – 20 больных, 36 глаз (12 мужчин, 8 женщин); 75 лет и более – 5 больных, 10 глаз (2 мужчин, 3 женщины); длительность заболевания: до 5 лет – 1 больной, 1 глаз; 5–9 лет – 7 больных, 12 глаз; 10–14 лет – 15 больных, 28 глаз; 15–19 лет – 6 больных, 11 глаз; более 20 лет – 2 больных, 4 глаза.
У всех больных определяли уровень гликированного гемоглобина Hb A1C, проводили офтальмологическую диагностику: проверка остроты зрения, исследование полей зрения (на периметре Гольдмана), исследование переднего отрезка глаза, биомикроскопия хрусталика и стекловидного тела с помощью щелевой лампы и офтальмоскопия. Дополнительно проводили оптическую когерентную томографию, исследовали глазное дно с помощью сканирующей лазерной фундус-камеры фирмы «Zeiss». Все исследования повторяли через каждые 2 месяца и полученные результаты сопоставляли с ранее имеющимися данными.
Оценка наличия и тяжести диабетической ретинопатии проводилась по классификационной шкале ETDRS (Early Treatment Diabetic Retinopathy Scale) [27], являющейся модификацией градационной шкалы Airlie House [28]. По этой шкале уровень 10 соответствует отсутствию диабетической ретинопатии; уровень 20 (наличие только микроангиопатий) – слабовыраженной (невыраженной) диабетической ретинопатии; уровни 35–47 – умеренной непролиферативной диабетической ретинопатии с субпоказателями относительно правила 4 : 2 : 1 (см. ниже); уровень 53 А-Е – выраженной непролиферативной диабетической ретинопатии, соответствующей правилу 4 : 2 : 1; начиная с уровня 61 (неоваскуляризация, наличие кровоизлияний в стекловидное тело и т. п.) – пролиферативой диабетической ретинопатии различной степени тяжести и риска относительной полной потери зрения.
Учитывали геморрагии, микроаневризмы, «твердые» и «мягкие» экссудаты, интраретинальные микроваскулярные нарушения, четкообразность вен, новообразование сосудов, кровоизлияния в стекловидное тело, преретинальные кровоизлияния, фиброзную пролиферацию и т. п.
В случаях, когда распознавание интраретинальных микроваскулярных нарушений и «четкообразных» вен было затруднительным, суррогатные маркеры, такие как геморрагии и/или микроаневризмы были взяты за критерии оценки. Четвертый уровень тяжести диабетической ретинопатии – выраженная непролиферативная диабетическая ретинопатия – диагностировали по правилу ETDRS 4 : 2 : 1 – наличие выраженных геморрагий в 4 квадрантах; или «четкообразные» вены в двух квадрантах; или интраретинальные микроваскулярные нарушения в одном квадранте. Глаза, которые не могли быть градированы из-за помутнения хрусталика, стекловидного тела, фтизиса, энуклеации и т. п., с самого начала классифицировались как «не поддающиеся» градации и исключались из исследования. У каждого пациента при оценке результатов испытания прежде всего учитывалось состояние сетчатки наиболее пораженного глаза. Результаты оценивались, исходя из изменения остроты зрения и состояния сетчатки как (+) – улучшение; (–) – ухудшение; (0) – без изменений. Критерием оценки принимали шаг шкалы ETDRS. Проводящий оценку специалист не обладал информацией относительно того, в какую группу (лечебную или плацебо) входил больной («слепая» оценка). Статистическая обработка проводилась с использованием критерия Фишера.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Динамика изменений остроты зрения и состояния сетчатки в лечебной (глазные капли с N-ацетилкарнозином) и контрольной (плацебо) группах больных с диабетической ретинопатией к концу 6-месячного срока клинического испытания представлены в таблице 1.

Положительный эффект и стабилизация процесса в лечебной группе наблюдались значительно чаще, чем в группе плацебо (различия статистически достоверны, р < 0,001), в то время как ухудшение в лечебной группе отмечалось существенно реже (различия достоверны, р < 0,001). Вместе с тем, различия в уровне гликированного гемоглобина Hb A1C в лечебной и контрольной группах были статистически недостоверными (р > 0,05), это свидетельствует о том, что качество гликемического контроля в группах существенно не отличалось и этот фактор не оказывал влияния на результаты клинического испытания. Анализ полученных данных показывает, что при применении N-ацетилкарнозина наблюдается снижение относительного риска прогрессирования диабетической ретинопатии у данного контингента больных более чем в 10 раз. В то же время применение глазных капель с N-ацетилкарнозином не вызывало побочных реакций.
Таким образом, глазные капли с N-ацетилкарнозином (импортируемые под названием Clarastill производства фирмы «Bruschettini», Италия) являются эффективным средством профилактики развития и прогрессирования диабетической ретинопатии. Поскольку развитие диабетической ретинопатии рано или поздно наблюдается у подавляющего большинства больных, а также учитывая проблемы лечения этой патологии, рекомендуется как можно более раннее назначение глазных капель с N-ацетилкарнозином больным с сахарным диабетом. В случаях развившейся диабетической ретинопатии целесообразно долгосрочное закапывание капель с N-ацетилкарнозином для стабилизации процесса, предотвращения ее дальнейшего прогрессирования, а в ряде случаев и для достижения регрессии уже развившихся патологических изменений сетчатки. Учитывая выраженные антиоксидантные, цитопротективные, трофические и гидратирующие свойства N-ацетилкарнозина, целесообразно его назначение до и после проведения лазерной коагуляции, а также для сохранения остаточного зрения в далеко зашедших случаях диабетической ретинопатии.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
- Бородай А.В., Сабурова Г.Ш., Ишунина А.М. Танакан в лечении диабетических микроангиопатий. VII съезд офтальмологов России. Тез. докл., ч. 1, М., 2000. с. 304−305.
- Галилеева В.В., Киселева О.М. Применение антиоксиданта мексидола у больных с диабетической ретинопатией. VII съезд офтальмологов России. Тез. докл., ч. 2, М., 2000, с. 425–426.
- Евграфов В.Ю. Диабетическая ретинопатия: патогенез, диагностика, лечение. Автореф. дис. ... докт. мед. наук. М., 1996, 47 с.
- Ефремова Л.Л. Применение препарата системной энзимотерапии вобэнзима в лечении гемофтальмов и иридоциклитов. Автореф. дис. ... канд. мед. наук. Ростов-на-Дону, 2000, 24 с.
- Зуева М.В., Цапенко И.В., Кубатиев А.А., Недосугова Л.В., Волковой А.К., Бегляров Д.А. Влияние препарата Диквертина на течение диабетической ретинопатии. VII съезд офтальмологов России. Тез. докл. ч. 2, М., 2000, с. 440–441.
- Ильенков С.С., Вайник Д.Е., Ланин С.Н., Леонова Л.Л., Лазаренко В.И. Эффективность ксантинола никотината при диабетической ретинопатии. Вопросы офтальмоэндокринологии и сосудистой патологии глаз. Мат. науч. практ. конф. офтальмологов и эндокринологов. Красноярск, 1999, с. 32–38.
- Ильенков С.С., Вайник Д.Е. Изменения гемореологических показателей у больных диабетической ретинопатией и медикаментозные способы их коррекции. VII съезд офтальмологов России. Тез. докл., ч. 1, М., 2000, с. 313–314.
- Крупчатникова О.В., Денисов Л.Н. Вобэнзим в комплексном лечении сосудистых и посттравматических поражений органа зрения. VII съезд офтальмологов России. Тез. докл. ч. 1, М., 2000, с. 317.
- Крутенков О.А., Евграфов В.Ю. Влияние локального введения тромболитиков и эмоксипина на остроту зрения и показатели периметрии у больных диабетической ретинопатией. Мат. II Евро-Азиатской конференции по офтальмохирургии, ч. 2, разд. 6–12, Екатеринбург, 2001, с. 326–327.
- Мареев В.Ю. Четверть века эры ингибиторов АПФ в кардиологии. Русский медицинский журнал, 2000, 15–16, с. 602–609.
- Нудьга Л.И. Комплексное лечение диабетической ретинопатии. VII съезд офтальмологов России. Тез. докл., ч. 2, М., 2000, с. 472–473.
- Скрипка В.П., Тур А.Н., Угай Н.А. Эффективность системной энзимотерапии в лечении больных с диабетической ретинопатией. VII съезд офтальмологов России. Тез. докл., ч. 1, М., 2000, с. 330.
- Скуратова Т.М. Использование препарата диквертин для лечения диабетической ангиопатии. Вопросы офтальмоэндокринологии и сосудистой патологии глаз. Мат. науч. практ. конф. офтальмологов и эндокринологов. Красноярск, 1999, с. 38–39.
- Скуратова Т.М., Ульданов В.Г., Золотавин В.В., Пьянков В.З. Опыт применения препарата диквертин в клинической практике у больных с диабетической ангиопатией. Офтальмология Якутии на рубеже веков. Мат. науч. практ. конф. офтальмологов, посвященной 75-летию службы. Якутск, 2000, с. 130–131.
- Сорокин Е.Л. Оптимизация лечения манифестных форм диабетической ретинопатии. Мат. II Евро-Азиатской конференции по офтальмохирургии, ч. 1, разд. 1–5. Екатеринбург, 2001, с. 184–185.
- Трофимова С.В. Применение пептидных биорегуляторов при лечении диабетической ретинопатии. Автореф. дис. ... канд. мед. наук, СПб., 1999, 20 с.
- Хавинсон В.Х., Трофимова С.В. Биорегуляторные пептиды в лечении диабетической ретинопатии. VII съезд офтальмологов России. Тез. докл. ч. 1, М., 2000.
- Aiello L.P. The potential role of PKC beta in diabetic retinopathy and macular edema. Surv. Ophthalmol., 2002. 47, suppl. 2, p. S263–S269.
- American Academy of Ophthalmology. Preferred Practice Pattern: Diabetic Retinopathy 1998, San Francisco, Calif: American Academy of Ophthalmology, 1998.
- Babizhayev M.A., Seguin M.C., Gueyne J. et al. L-carnosine (beta-alanyl-L-histidine) and carcinine (beta-alanylhistamine) act as natural antioxidants with hydroxyl-radical-scavenging and lipid peroxidase activities. Biochem., J., 1994, 304: 509−16.
- Babizhayev M.A., Yermakova V.N., Sakina N.L. et al. N-acetylcarnosine is a prodrug of L-carnosine in ophthalmic application as antioxidant. Clin. Chim. Acta, 1996, 254:1–21.
- Boldyrev A.A., Dupin A.M., Bunin A.Y. et al. The antioxidative properties of carnosine, a natural histidine containing dipeptide. Biochem. Int., 1987, 15: 1105−13.
- Chaturvedi N., Sjolie A.K., Stephenson J.M. et al. Effect of lisinopril on progression of retinopathy in normotensive people with type I diabetes. Lancet, 1998, 351, p. 28–31.
- Diabetic Retinopathy Research Group. Photocoagulation treatment of proliferative diabetic retinopathy: clinical application of diabetic retinopathy study (DRS) findings, DRS report number 8. Ophthalmology, 1981, 88:583−600.
- Early Treatment Diabetic Retinopathy Study Research Group. Early photocoagulation for diabetic retinopathy: ETDRS report 9. Ophthalmology, 1991, 98 (suppl):766−785.
- Early Treatment Diabetic Retinopathy Study Research Group. Effects of aspirin treatment of diabetic retinopathy. ETDRS Report 8. Ophthalmology, 1991, 98, p. 757–765.
- Early Treatment Diabetic Retinopathy Study Research Group. Fundus photographic risk factors for progression of diabetic retinopathy: ETDRS report number 12. Ophthalmology, 1991, 98:823−833.
- Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs: an extension of the modified Airlie House classification: ETDRS report number 10. Ophthalmology, 1991, 98:786−806.
- Early Treatment Diabetic Retinopathy Study Research Group. Photocoagulation for diabetic macular edema. ETDRS report 1. Arch. Ophthalmol, 1985, 103:1796–806.
- Expert Committee on the Diagnosis and Classification of Diabetes Mellitus. Report of the expert committee on the diagnosis and classification of diabetes mellitus. Diabetes Care, 1997, 20:1183−1197.
- Gardner T.W., Eller A.W., Friberg T.R. et al. Antihistamines reduce blood-retinal barrier permeability in type I (insulin-dependent) diabetic patients with non-proliferative diabetic retinopathy: A pilot study, Retina, 1995, 15, p. 134–140.
- Grant M.B., Cooper–DeHoff R., Mames R.N. et al. The efficacy of octreotide in the therapy of severe non-proliferative and early proliferative diabetic retinopathy. A randomized controlled study. Diabetes Care, 2000, 23, p. 504–509.
- Grant MB, Mames RN, Fitzgerald C, Hazariwala KM, Cooper-DeHoff R. et al. The efficacy of octreotide in the therapy of severe non-proliferative and early proliferative diabetic retinopathy: a randomized controlled study. Diabetes Care, 2000, 23: 504−509.
- Gulewitsch, W., Amiradzibi, S. Uber das carnosin, eine neue organische Base des Fleischextraktes. Ber. Deutch. Chem. Ges., 1900, 33, p.1902−1903.
- Harding S., Greenwood R., Aldington S. et al. Grading and disease management in national screening for diabetic retinopathy in England and Wales. Diabet. Med., 2003, 20:965–71.
- Massin P.G. Intravitreal triamcinolone acetonide for diabetic diffuse macular edema. Program and abstracts of the American Academy of Ophthalmology 2002 Annual Meeting, October 20–23, 2002, Orlando, Florida.
- Mayer-Davis E.J., Bell R.A., Reboussin B.A., Rushing J., Marshall J.A., Hamman R.F. Antioxydant nutritient intake and diabetic retinopathy. The San Luis Valley Diabetes Study. Ophthalmology, 1998, 105, p. 2264–2270.
- Mogensen C.E. Diabetic complications and early treatment using ACE-inhibitors: concluding remarks. Journal of Diabetes and its Complications, 1996, 10(3), p. 151–153.
- Pearson P.A. Fluocinolone acetonide intravitreal implant in patients with diabetic macular edema. Program and abstracts of the American Academy of Ophthalmology 2002 Annual Meeting, October 20–23, 2002, Orlando, Florida.
- Porta M, Allione A. Current approaches and perspectives in the medical treatment of diabetic retinopathy. Pharmacol. Ther., 2004;103:167–77.
- Poulsen J.D. Diabetes and anterior pituitary deficiency. Diabetes, 1953, 2, p. 7–12.
- Sorbinil Retinopathy Trial Research Group. A randomized trial of Sorbinil, an aldose reductase inhibitor in diabetic retinopathy. Arch. Ophthalmol., 1990, 108, p.1234–1244.
- Stefansson E., Bek T., Porta M. et al. Screening and prevention of diabetic blindness. Acta Ophthalmol. Scand., 2000;78:374–85.
- Stratton I.M., Kohner E.M., Aldington S.J. et al. UKPDS 50: risk factors for incidence and progression of retinopathy in type II diabetes over 6 years from diagnosis. Diabetologia, 2001;44:156–63.
- TDRSR Group. Photocoagulation treatment of proliferative diabetic retinopathy. Clinical ap-plication of Diabetic Retinopathy Study (DRS) findings, DRS Report 8, Ophthalmology, 1981;88:583–600.
- The DAMAD Study Group. Effect of aspirin alone and aspirin plus dipyridamole in early diabetic reinopathy. A multicentre randomized controlled clinical trial. Diabetes, 1989, 38, p. 491–498.
- The DCCT Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N. Engl. J. Med., 1993;329:977−986.
- The DIabetic REtinopathy Candesartan Trials (DIRECT) programme. Diabetes & Metabo lism, 2001, 27, suppl. 2, p. 2S4.
- The Eye Diseases Prevalence Research Group. The prevalence of diabetic retinopathy among adults in the United States. Arch. Ophthalmol. 2004, 122:552–563.
- The TIMAD Study Group. Ticlopidine treatment reduces the progression of nonproliferative diabetic retinopathy. Arch. Ophthalmol., 1990, 108. p. 1577.
- Trautner C., Icks A., Haastert B. et al. Incidence of blindness in relation to diabetes. A popula-tion-based study. Diabetes Care, 1997, 20:1147–53.
- U.K. Prospective Diabetes Study Group: Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet, 1998, 352:837−853.
- Understanding diabetic retinopathy by Pardianto G. et al. Mimbar Ilmiah Oftalmologi, Indonesia.2005, 2:65−6.
- Wahren, J., Ekberg, K., Jörnval H. C-peptide is a bioactive peptide. Diabetologia, 2007, 50, 3, p.60−63.
- Younis N., Broadbent D.M., James M. et al. Current status of screening for diabetic retinopathy in the UK. Diabet. Med., 2002, 19, 4:44–9.
- Zimmet P., Alberti K.G., Shaw J. Global and societal implications of the diabetes epidemic. Nature, 2001, 414:782–7.
Стаття надійшла в редакцію 21.09.2017 р.
Рецензія на статтю надійшла в редакцію 05.10.2017 р.