- Автор: Super User
- Опубліковано: 14 липня 2019
- Перегляди: 6876
УДК 617.735–007.281–089
Інгрід Крейссіг, MD, Prof. h. c.
Кафедра офтальмології, Медичний факультет Мангейма, Гейдельберзький університет, м. Мангейм, Німеччина
Ключова лекція – присвячена Харві Лінкоффу, MD, який покинув цей світ 25 листопада 2017 року. Була представлена на Міжнародній конференції «Судинні та ендокринні патології органа зору» в Києві (Україна, 1 березня 2018 року).
У статті розглянуто техніки для відновлення цілісності первинних розривів сітківки, які були розроблені за останні 85 років при повторних пошкодженнях сітківки.
Перший концептуальний прорив у лікуванні відшарувань сітківки належить Гоніну Ж. в 1930 році [1]. Він вважав, що причиною відшарувань сітківки є розрив. Гонін Ж. спровокував процес запалення навколо розриву. Відсоток повторного прилягання сітківки зріс від 0 до 57 %. Однак більш детально виявити місце розриву було складно. Згодом, уже в 1931 році, Густ E. та Ліндер К. визначили первинну локалізацію розриву, виконавши значну кількість діатермокоагуляцій, як спосіб створити бар’єр – із заднього боку по відношенню до розриву, щоб запобігти повторному відшаруванню сітківки [2, 3]. У 1932 році Сафар К. [4] наклав короткі перфоруючі затискачі уздовж усього бар’єра чи поодинокі у напівциркляжі позаду від розриву та торкнувся їх діатермічним електродом, щоб створити перешкоду, або коагуляційний бар’єр.
Дренування проводили після видалення затискачів. З винайденням цієї бар’єрформуючої операції рівень повторного прилягання сітківки зріс до 70 %, однак випадки повторного відшарування все одно виникали. Це ставалося тому, що ретинальні розриви не були достатньо запломбовані.
Другий концептуальний прорив у лікуванні відшарувань сітківки розпочався завдяки Розенгрену Б. у 1938 році [5]. Він також обмежив ділянку розриву зоною коагуляцій, однак додатково, після дренування субретинальної рідини, помістив у середину ока повітряну бульбашку для тампонування розриву інтраокулярно. І справді, рівень повторного прилягання сітківки зріс до 77 %, а це в 1938 році було вже значним досягненням!
Незважаючи на успіхи, випадки повторного відшарування виникали знову. Це траплялося тому, що повітря у вітреальній порожнині надто швидко розсмоктувалося, що зумовлювало повторне підтікання розриву ще до розвитку достатньо сильної адгезії навколо нього. Інша проблема полягала, як уже зазначалося раніше, у труднощах визначити розташування розриву, тобто обмеження коагуляціями безпосередньо ділянки навколо розриву.
Отже, перевагу знову віддали мікрохірургічному методу з більшою кількістю коагуляцій. Чому? Щоб створити бар’єр позаду від розриву. Але в той же час було додано резекцію склери в ділянці коагуляцій та в подальшому пломбу вставлено в ділянку резекції з метою створення високої стіни. Щоб запобігти підтіканню рідини під розривом у майбутньому, додатково було сформовано кілька ліній коагуляції від пломби в напрямку до зубчастої лінії (рисунок 1).
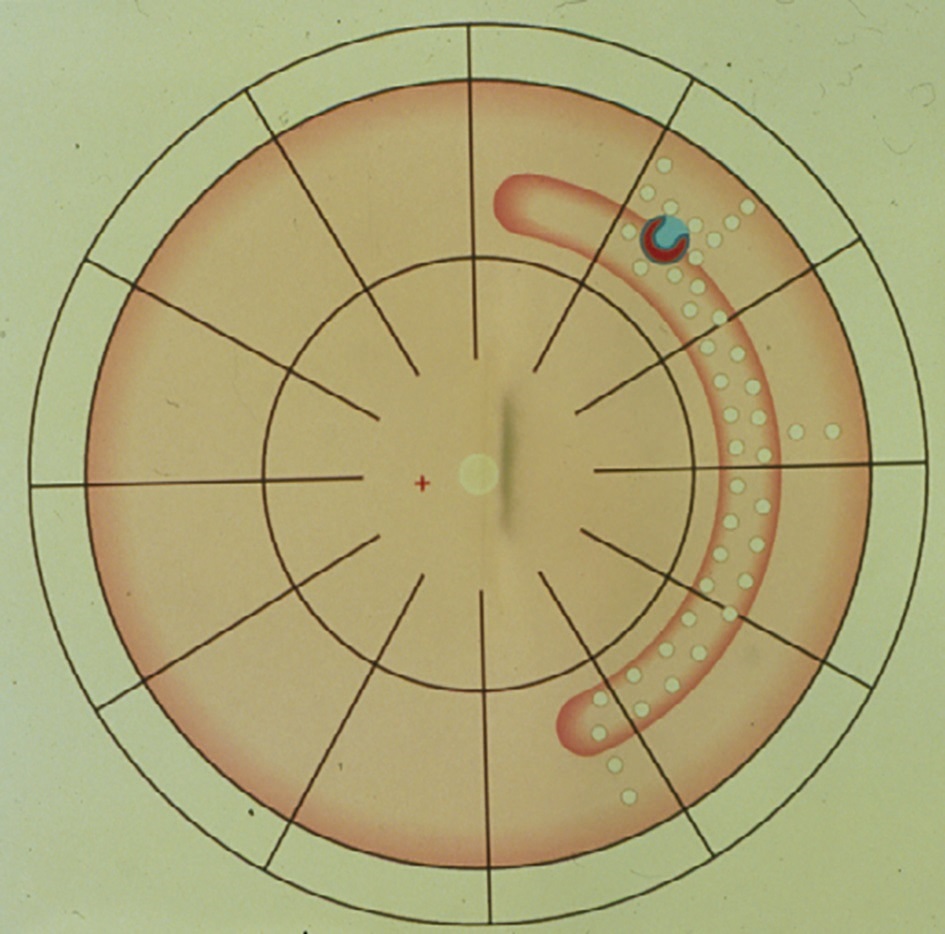
Рисунок 1. Пломба на сегменті з 12-ї до 5-ї години з розривом сітківки, що розташований на передньому краю пломби, обмеженої діатермічними коагуляціями; для запобігання подальшому підтіканню рідини під розривом виконано додакові коагуляції по всій пломбі та кілька коагуляційних бар’єрів у напрямку до зубчастого краю (From Primary Retinal Detachment: Options for Repair by Ingrid Kreissig (ed): Springer Berlin, Heidelberg, 2005, 9:179, Fig. 9.2a)
Оскільки розрив не був затампонований спереду (чого ще ми мали очікувати?), він починав підтікати знову, відшарування відбулося крізь коагуляційний бар’єр по нижній межі пломби, та, подолавши весь шлях, ініціювало повторне відшарування сітківки позаду (рисунок 2).
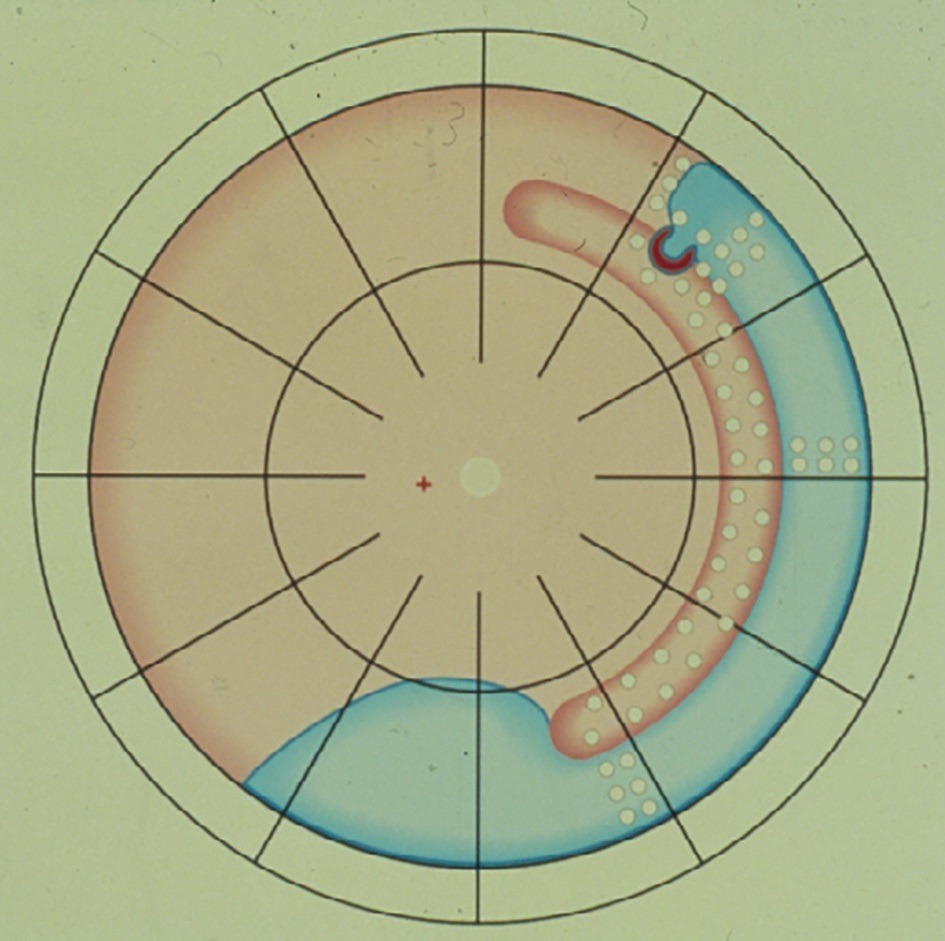
Рисунок 2. Розрив сітківки починає підтікати з передньої частини, що зумовлює повторне відшарування спереду від пломби, яке в подальшому перетинає всі можливі коагуляційні бар’єри та рухається в напрямку до задньої частини сітківки, що призводить до повторного відшарування (From Primary Retinal Detachment: Options for Repair by Ingrid Kreissig (ed): Springer Berlin, Heidelberg, 2005, 9:179, Fig. 9.2b)
Згодом, у 1953 році Щепенс С. Л. [6] представив циркулярну пломбу, або так званий циркляж. Цю операцію виконували з дренуванням субретинальної рідини.
Накладання циркляжу й досі залишається першою методикою вибору для відновлення цілісності сітківки в разі відшарувань (рисунок 3). Її суть полягає у створенні максимального бар’єра, що перешкоджає підтіканню рідини під розривом у задньому напрямку. З розробленням операції з накладанням циркляжу рівень прилягання сітківки зріс більш ніж на 80 %, однак сітківка реагує на ще підтікаючий розрив, якщо він не був затампонований достатньо, і це нагадує нам про основний чинник повторних відшарувань. Пізніше у 1977 році Прюетт Р. C. [7] додав клиноподібну пломбу до циркляжу для забезпечення повної тампонади розриву.
У декого з Вас може виникнути питання: коли потрібна повна тампонада розриву клиноподібною пломбою і навіщо циркляж все ще накладають?
Третій концептуальний прорив у лікуванні відшарувань сітківки відбувся завдяки Ернсту Кустодісу в 1953 році (рисунок 4) [8]. Він обмежив ділянку розриву після хірургічного втручання. Суть його методики полягала в застосуванні діатермії на всю товщу стінки та накладанні еластичної полівіолової пломби, фіксованої до склери в ділянці розриву, але спочатку операцію з приводу відшарування проводили без дренування субретинальної рідини. Але як це можливо?
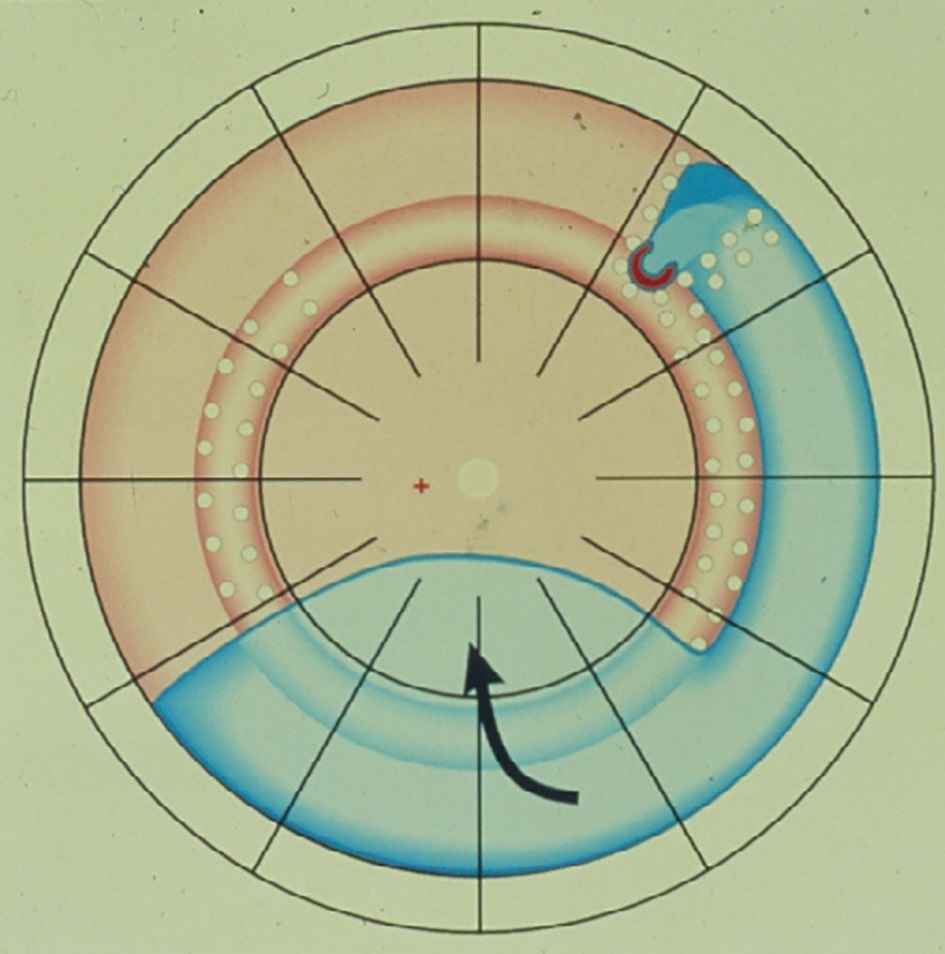
Рисунок 3. Циркулярна пломба (циркляж) з виконаними по всій її довжині коагуляціями та повторне відшарування спереду від неї, що розпочинається й опускається по передньому краю від пломби, перетинаючи коагуляційні бар’єри, але, враховуючи розташований позаду циркляж, значна кількість субретинальної рідини з більшим імпульсом прогресування у подальшому проходить крізь циркляж знизу та рухається по сітківці в задньому напрямку (From Primary Retinal Detachment: Options for Repair by Ingrid Kreissig (ed):Springer Berlin, Heidelberg, 2005, 9:180, Fig. 9.3с)
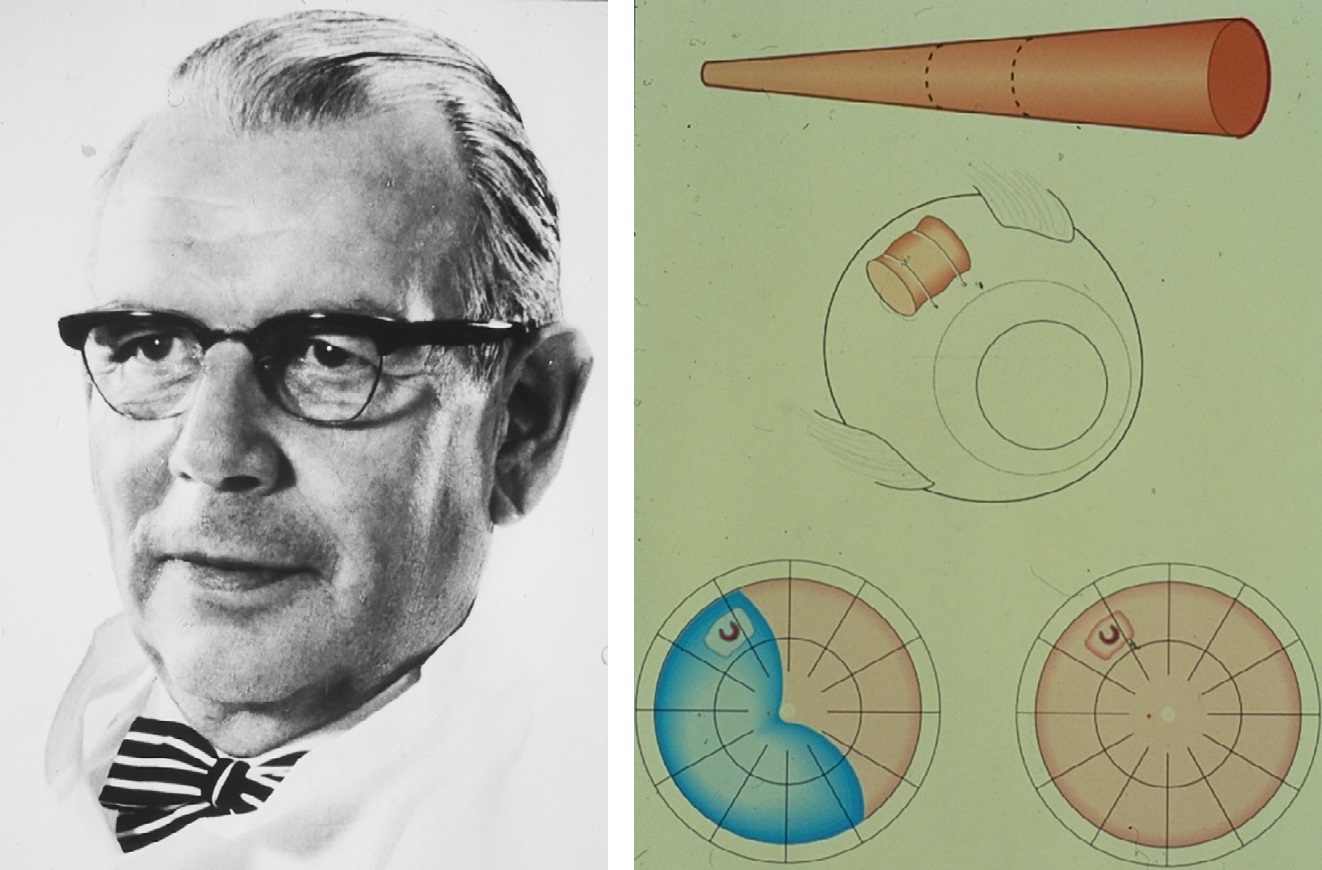
Рисунок 4. Ернст Кустодіс представив у 1954 році методику лікування відшарування сітківки з використанням еластичної полівіолової пломби, накладенням діатермії навколо розриву та без дренування субретинальної рідини. Тоді спостерігали серйозні післяопераційні ускладнення
Це стало реальним завдяки використанню еластичної пломби. Водночас відзначали розвиток серйозних неочікуваних ускладнень через токсичність полівіолової пломби разом з діатермією склери на всю товщину. Нещодавно були підгтовлені доповіді щодо розвитку післяопераційного склерального абсцесу, ендофтальміту та навіть енуклеації, що, на жаль, зумовило завершення використання методу Кустодіса в Європі і в Америці.
Однак не всі відмовилися від застосування цього методу в Америці, зокрема Харві Лінкофф у 1965 році (рисунок 5) [9, 10]. Він з відкритим до всього нового розумом був переконаний у раціональності підходу нового методу Кустодіса та в подальшому уникав доповідей про тяжкі післяопераційні ускладнення нової процедури.
У 1965 році Харві Лінкофф замінив еластичну полівіолову пломбу на еластичну губку з інертної тканини, використовував кріохірургічний метод та виконував діатермію, що зумовлювало розвиток некрозу [10].
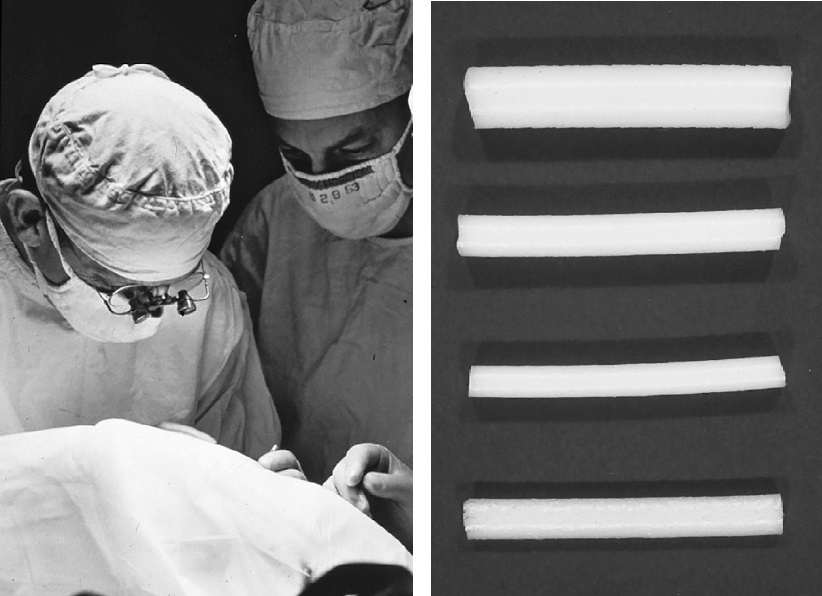
Рисунок 5. Харві Лінкофф представив у 1965 році модифікований метод Кустодіса із заміщенням діатермії кріохірургією, полівіолової пломби – еластичною губкою з інертної тканини та зміг обійтися завдяки цьому без дренування
Однак кріопексія не була повністю прийнята. Чому? Тому що були великі сумніви стосовно її адгезивної сили. З 1962 по 1972 рік Крейссіг І. працювала із Лінкоффом Х. у Нью-Йорку над питанням адгезивної сили кріопексії, відповідь на яке вони намагалися відтворити в численних експериментах на тваринах протягом 3 років [11, 12]. У процесі роботи 336 кролячих ока піддали впливу діатермії. За результатами було підтверджено, що адгезивна сила кріохірургічного втручання сильніша через 7 днів та потім досягає максимальної сили на 12-й день. Додатково було встановлено, що це можна виконати кріохірургічним шляхом за умови, якщо пошкодження наносяться під контролем офтальмоскопії.
Пошкодження легкого ступеня сприяють виникненню незначної адгезії, середнього ступеня – середній адгезії та значні пошкодження – сильній адгезії, що зумовлює можливість викликати адгезію різної сили.
Під час процедури хірургічного пломбування було обмежено зону розриву та дренування субретинальної рідини не проводили. Але пізніше встановили, що спонтанне повторне приєднання сітківки трапляється лише в післяопераційний період за умови, що розрив було виявлено та повністю запломбовано. Саме тому виявлення всіх розривів стає приорітетним у діагностиці, адже через це залежить успіх подальшого оперативного втручання без дренування субретинальної рідини.
Отже, після аналізу зображень 1000 випадків ретинальних відшарувань у 1971 році Лінкофф Х. і Гейзер Р. [13] розробили правила відносно того, де слід шукати дірки при первинному відшаруванні сітківки. Вони не втратили своєї цінності й досі в практичній діяльності кожного вітреоретинального хірурга (рисунок 6).
Згодом у 1996 році Лінкофф Х. і Крейссіг І. [14] встановили додаткові чотири правила, щоб знайти «пропущений» розрив на оці перед повторним хірургічним втручанням (рисунок 7).
Четвертий концептуальний прорив для відновлення відшарованої сітківки було здійснено вже після розроблення цих 8 правил. Відповідно до цих правил виявляли ретинальні розриви при первинних відшаруваннях або під час повторного оперативного втручання на оці.
Крім того, у 1975 році Лінкофф Х. і Крейссіг І. з’ясували, що розрив краще тампонується радіальною пломбою, ніж циркулярною, оскільки розташований позаду «риб’ячий рот» і переднє підтікання рідини під розрив можуть бути повністю перекриті радіальною пломбою (рисунок 8) [15]. У всіх випадках сітківку обробляли шляхом кріопексії без дренування.
За частотою використання на сьогодні мінімальне сегментарне пломбування без дренування, або мікрохірургія, для відновлення первинного відшарування сітківки посідає друге місце (рисунок 9). Цей метод полягає в проведенні кріопексії та ендотампонади губкою, обмеженою ділянкою розриву, без дренування субретинальної рідини [16, 17]. Частота повторного прилягання сітківки після першої операції зростає до 93 % після повторної – до 97 %. Після виконання такої локальної процедури без дренування розвиток проліферативної вітреоретинопатії (ПВР) як пізнього ускладнення зменшується до 1,9 %.
Для зменшення травмування тканин під час операції та в подальшому в 1979 році пломбу з губки було замінено на тимчасову балонну еластичну пломбу без накладання внутрішніх склеральних швів для фіксації та без дренування субретинальної рідини. Це найменш травматична процедура.
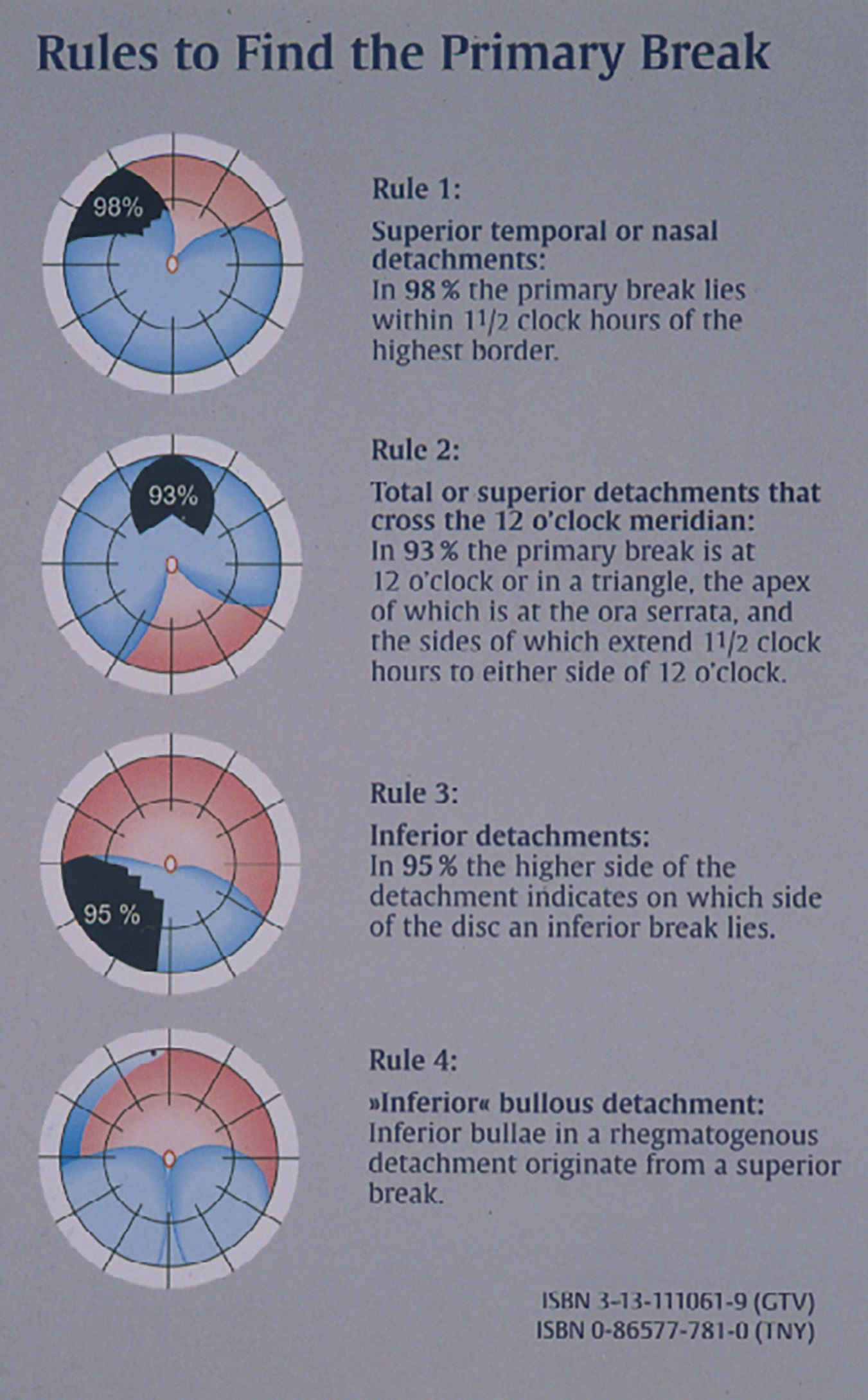
Рисунок 6. Правила виявлення первинного розриву при відшаруванні сітківки (From A Practical Guide to Minimal Surgery for Retinal Detachment: Diagnostics, Segmental Buckling without Drainage, Case Presentations by Ingrid Kreissig: Thieme, Stuttgart, New York, 2000; back cover)

Рисунок 7. Чотири правила, щоб відшукати «пропущений» розрив під час реоперації з приводу відшарування сітківки (From A Practical Guide to Minimal Surgery for Retinal Detachment: Temporary Tamponades with Balloon and Gases without Drainage, Buckling versus Gases versus Vitrectomy, Reoperation, Case Presentations by Ingrid Kreissig, 2000, back cover)
а)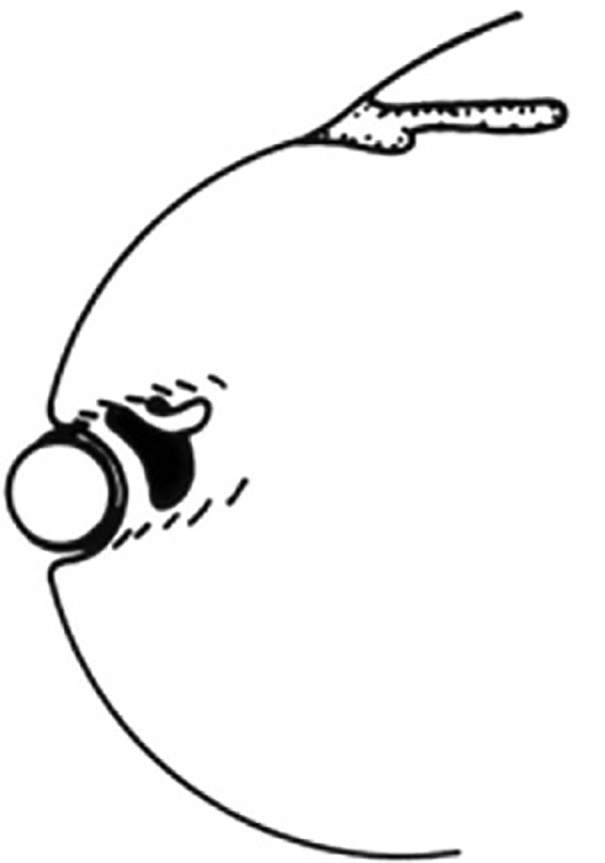
б)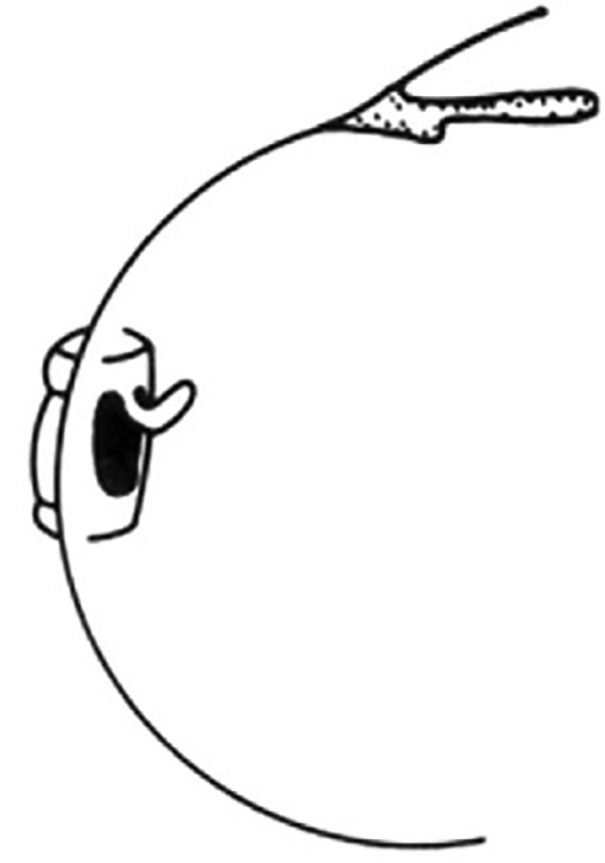
Рисунок 8. Накладання сегментарної пломби шляхом тампонади підковоподібного розриву: при використанні циркулярної пломби (А) підковоподібний розрив не буде повністю затампонованим. Оболонка в ділянці майбутньої тракції розміщена спереду від пломби. Крім того, є ризик утворення задньої радіальної брижі у вигляді «риб’ячого рота», з подальшим підтіканням рідини під розрив. Застосування короткої радіальної пломби (Б) забезпечує найоптимальнішу тампонаду підковоподібного розриву. Розрив повністю «вписується» у межі пломби, тобто така контракція заднього розриву за типом «риб’ячого рота» забезпечує найкраще прилягання оболонки, запобігаючи розвитку передньої вітреальної тракції (From A Practical Guide to Minimal Surgery for Retinal detachment: Diagnostics, Segmental Buckling without Drainage, Case Presentations by Ingrid Kreissig. Thieme, Stuttgart, New York: Thieme, Stuttgart, New York, 2000;8:141, Fig. 8.6)

Рисунок 9. Мінімальне сегментарне пломбування без дренажу, так звана екстраокулярна мікрохірургія: лікування полягає в тому, щоб обмежити площину самого розриву незалежно від довжини відшарування. Мале (з верхівкою лівіше) та більш значне відшарування (з верхівкою правіше) є результатом однакового підковоподібного розриву на 1-й годині. Лікування обох різновидів розриву однакове і зводиться до пломбування дірки по всій поверхні сегментарною губкою (як зображено) або встановленим на певний час балоном без дренування субретинальної рідини (From A Practical Guide to Minimal Surgery for Retinal Detachment: Diagnostics, Segmental Buckling without Drainage, Case Presentations by Ingrid Kreissig: Thieme, Stuttgart, New York, 2000, part of front cover)
Балон Лінкоффа – Крейссіг був презентований як п’ятий концептуальний прорив у лікуванні відшарувань сітківки (рисунок 10) [18].
Балонна операція – третя за частотою виконання процедура для відновлення первинного відшарування сітківки. Процедуру проведення операції було вдосконалено: 1) пломбу не фіксують жодними швами; 2) балонну пломбу видаляють із середини ока через тиждень. Така операція показана в разі наявного відшарування з 1 розривом чи групою розривів, які розташовані в межах 1-ї години (рисунок 11). Відзначають такі результати після 1 балонної операції: повторне прилягання – у 93 % випадків, після видалення балона – повторне відшарування спостерігають у перші 6 місяців у 2 % прооперованих, однак після реоперації повторне прилягання сітківки зростає вже до 99 % випадків протягом наступних 36 місяців [19]. Після цієї атравматичної балонної операції ризик післяопераційної ПВР у подальшому знизився до 0,2 %.
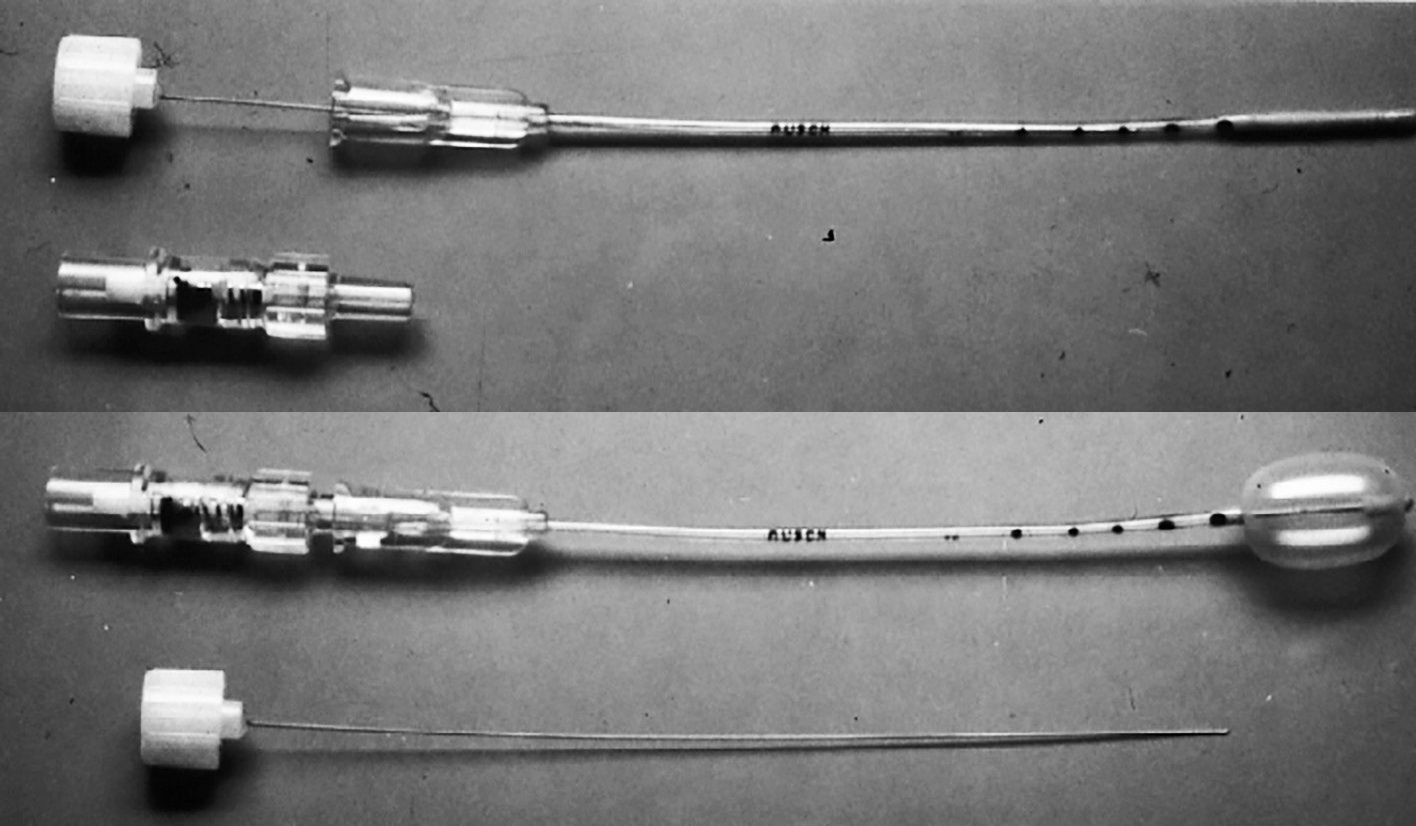
Рисунок 10. Балон Лінкоффа – Крейссіг: балон має металевий стрижень, що полегшує проникнення в парабульбарний простір та калібрати (чорні відмітки) на трубі, щоб встановити балон у парабульбарному просторі з більшою точністю. Негофрований балонний катетер зі стрижнем; під ним адаптер (зверху). Надувна куля (0,75 мл стерильної води) з клапаном, що сам закривається після введення; під ним стржень, який можна вилучити (нижня частина) (From A Practical Guide to Minimal Surgery for Retinal Detachment: Temporary Tamponades with Balloon and Gases without Drainage, Buckling versus Gases versus Vitrectomy, Reoperation, Case Presentations by Ingrid Kreissig: Thieme Stuttgart, New York, 2000, 9: 5, Fig. 9.1)
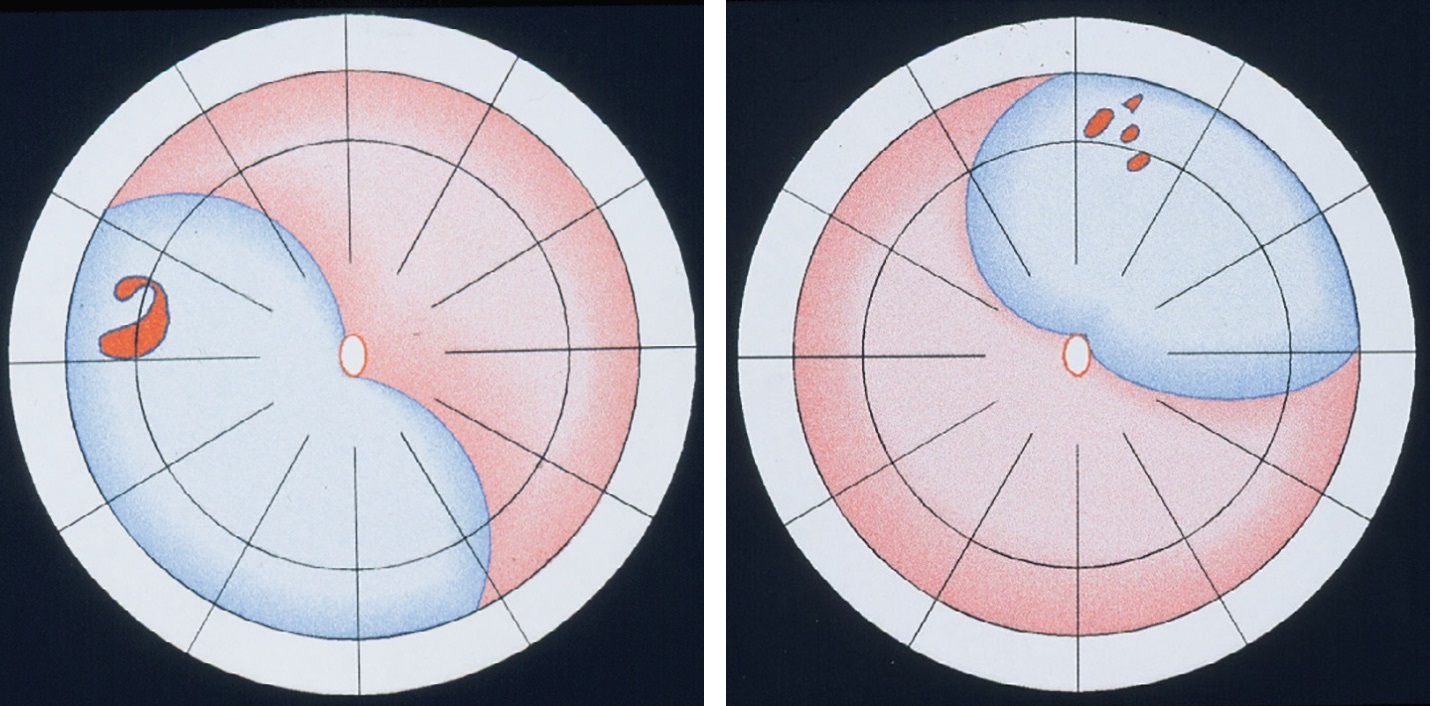
Рисунок 11. Показання до операції з використанням балона: відшарування сітківки, спровоковані одиничними дірками (зверху) чи групою розривів, розташованих поряд (знизу), що не виходить за межі 1-ї години або 6 мм по екватору і який може бути розташований на будь-якій годині умовного циферблату, тобто вище чи нижче, але має бути на передній 2/3 очного яблука (From A Practical Guide to Minimal Surgery for Retinal Detachment: Temporary Tamponades with Balloon and Gases without Drainage, Buckling versus Gases versus Vitrectomy, Reoperation, Case Presentations by Ingrid Kreissig: Thieme Stuttgart, New York, 2000, 9: 6, Fig. 9.12)
Однак у разі великих розривів сегментарне пломбування виявилося неефективним. Накладання довгої циркулярної пломби спричинювало констрикцію очного яблука з підтіканням у новоутворених радіальних складках, що зумовлювало розвиток повторного заднього відшарування. Едвард Нортон (1973) разом з Харві Лінкоффом (1974) представили спосіб тампонади великих розривів внутрішньоочною газовою бульбашкою [20, 21]. Після дренування субретинальної рідини всередину ока було виконано ін’єкцію газу SF6, а межі розриву запломбовано шляхом кріопексії чи лазер-коагуляції після повторного прилягання (рисунок 12). У результаті цієї операції дренування знову втратило свій сенс, адже його виконували перед уведенням газу, щоб забезпечити достатню кількість місця для останнього.
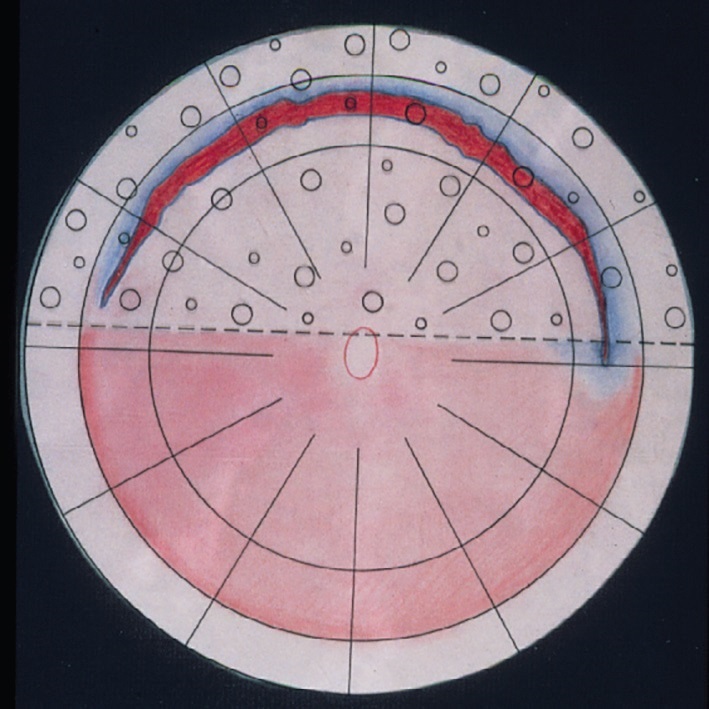
Рисунок 12. Газова бульбашка гексафториду сірки після дренування субретинальної рідини як метод інтраокулярної тампонади повторного відшарування великих розривів при відшаруванні сітківки
Шостий концептуальний прорив у відновленні відшарувань сітківки належить Інгрід Крейссіг у 1979 році [22–24] з виконанням операції, під час якої було введено розширюючий газ у середину ока без дренування субретинальної рідини. З 1974 року вона почала шукати можливість підтримати концепцію бездренажної операції з газовою ендотампонадою. Після виконання компресії ока стало можливим уведення всередину 0,4 мл гексафториду сірки без попереднього дренування, однак поки газ перебував усередині, інтраокулярний об’єм зріс удвічі – до 0,8 мл. Операцію з використанням газової ендотампонади без дренування виконували в разі відшарувань сітківки з великими дірками та задніми розривами, але ПВР стрімко зростала (таблиця 1).
Таблиця 1. Операція без дренування субретинальної рідини з використанням розширювального газу як метод лікування проблемних відшарувань сітківки (From Clinical experience with SF6-gas in detachment surgery by Ingrid Kreissig. Ber Dtsch Opthalmol Ges. 1979;76:553–560)
|
Відшарування |
n |
Прилягання |
ПВР |
| Гігантські розриви (75–195°) |
9 |
6 |
3 |
| Задні розриви |
3 |
3 |
– |
| ПВР-відшарування |
3 |
– |
3 |
| Усього | 15 | 9 | 6 (40 %) |
Однак операцію без дренування з використанням розширювального газу було розроблено для відшарувань із розривами тяжкого ступеня, а не для відшарувань з простими розривами. Чому? Тому що, по-перше, вірогідність розвитку післяопераційного ПВР після виконання ендотампонади ока газом була занадто високою і, по-друге, вже була доступна процедура балонної тампонади з практично відсутніми випадками ПВР (вірогідність виникнення близько 0,2 % в порівнянні).
Методику операції без дренування з використанням розширювального газу, що була призначена для складних розривів, у подальшому було покращено з презентацією перфторкарбонового газу проф. Харві Лінкоффом та його командою у 1980 році [25]. Швидкість розширення різних перфторвуглецевих газів є такою: близько 2× для тетрафторметану та гексафториду сірки, інші гази – у межах від 3,3× до 5× від їх початкового об’єму (рисунок 13) [25]. Проте що більша у газу здатність до розширення, то довший час його перебування в середині ока, що, як і слід було очікувати, впливає на підвищення ризику розвитку ПВР у пацієнта (рисунок 14) [26].
Незважаючи на вищий ризик післяопераційної ПВР після введення газу в середину ока, операція без дренування з використанням розширювального газу, розроблена Крейссіг І. у 1979 році, була повторно представлена Домінгезом А. [27] та Хілтоном Г. [28] у 1986 році, але вже під назвою пневматичної ретинопексії. Відтоді її виконували у разі відшарувань легкого ступеня тяжкості.
Пневматична ретинопексія є третім хірургічним методом за частотою використання на сьогодні для відновлення первинних відшарувань сітківки. Частота повторних прилягань після пневматичної ретинопексії для відшарувань легкого ступеня тяжкості становить близько 91 %, але після зникнення газу вона зменшується до 80 %, а після кількох повторних операцій знову зростає до 99 %. Як ускладнення, після газової ендотампонади ока можуть розвинутися: нові розриви у 15 % та післяопераційна ПВР у 14 % випадків.
Сьомий концептуальний прорив у відновленні ретинальних відшарувань був виконаний Робетом Мачемером у 1972 році [29], який представив вітректомію та відкрив її для відшарувань з ПВР (рисунок 15).
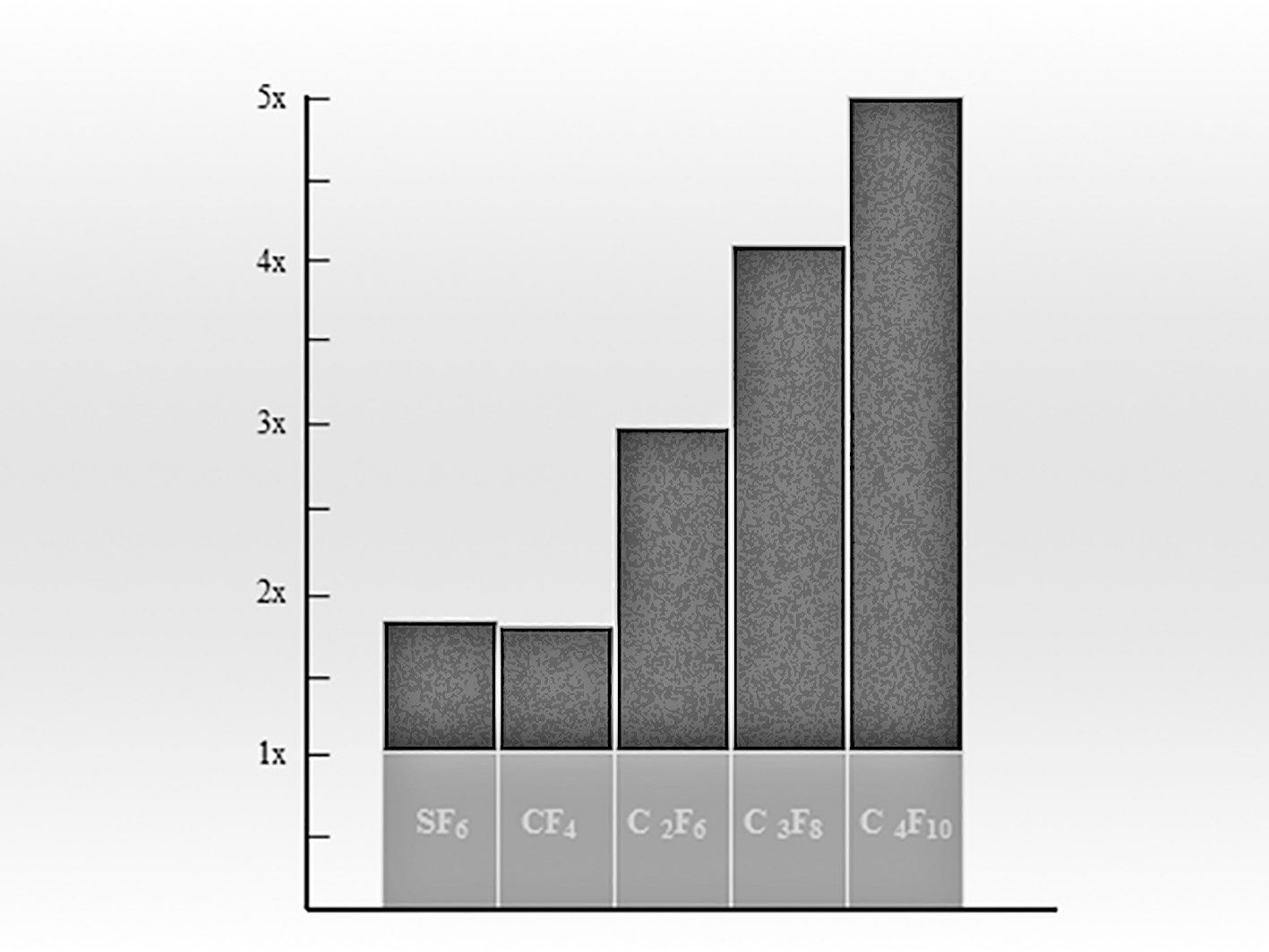
Рисунок 13. Розширення 4 прямоланцюжковими перфторкарбоновими газами та гесафторидом сірки в очах пацієнтів: гексафторид сірки та тетрафторметан мають коефіцієнт розширення 1,9×, гексафторетан – 3,3×, октафторпропан – 4×, перфторбутан – 5× (From A Practical Guide to Minimal Surgery for Retinal Detachment: Temporary Tamponades with Balloon and Gases without Drainage, Buckling versus Gases versus Vitrectomy, Reoperation, Case Presentations by Ingrid Kreissig: Thieme Stuttgart, New York, 2000, 10: 130, Fig. 10.9)
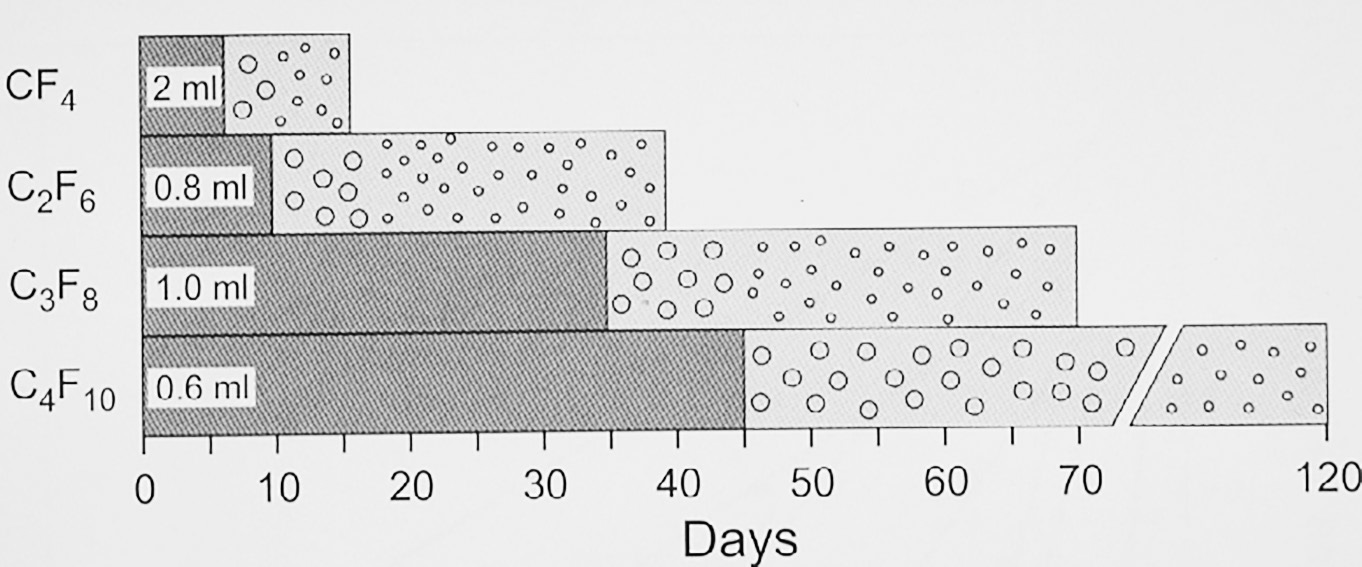
Рисунок 14. Час зникнення 4 прямоланцюжкових газів перфторкарбону в очах пацієнтів: ліва частина кожного стовпчика (темний сірий) вказує на те, скільки часу знадобилося розширювальному газу, щоб досягти половини бажаного об’єму. Напівжиття тетрафторметану коливається в межах 6 днів, гексафторетану – близько 10 днів, перфторпропану – від 24 до 35 днів, октафторпропану – близько 45 днів (From A Practical Guide to Minimal Surgery for Retinal Detachment: Temporary Tamponades with Balloon and Gases without Drainage, Buckling versus Gases versus Vitrectomy, Reoperation, Case Presentations by Ingrid Kreissig: Thieme Stuttgart, New York, 2000, 10: 125, Fig. 10.6)
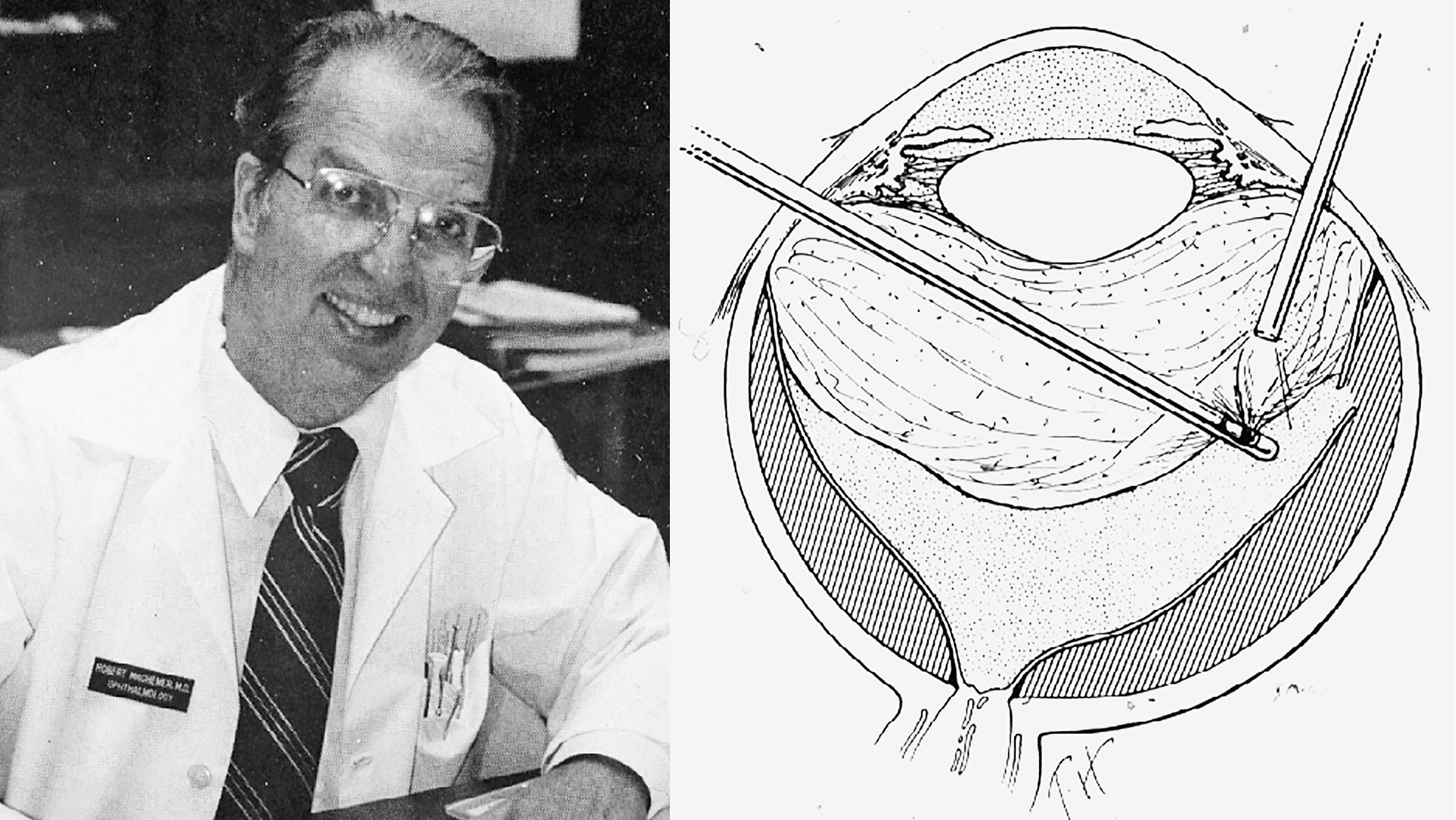
Рисунок 15. Роберт Мачемер, який презентував вітректомію для розривів з ПВР у 1972 році
Після 3-річного тренування в Нью-Йорку з Харві Лінкоффом у 1975 році у Бонні ми отримали перший результат – вітректомічне обладнання було транспортоване із США до Європи. У той час Інгрід Крейссіг була поглиблена в розробку методик мінімального сегментарного пломбування без дренування з мінімізацію ускладнень. Як наслідок, у неї не траплялося великої кількості випадків з післяопераційною ПВР, які могли б стати показаннями для проведення вітректомії, а також перфоративних пошкоджень, щоб виконувати повторну вітректомію з метою їх усунення. Тому пацієнти зі сторонніми тілами в очах та наявністю перфорацій були спрямовані до Невбуера в Кологні, у 12 мілях північніше від Бонна, де він відкрив нову техніку для виявлення локалізації та видалення неметалевих внутрішньоочних сторонніх тіл. Інгрід Крейссіг, яка контактувала з Невбуером та його керівником Клаусом Хейманом в Кологні, запропонувала їм свій новий пристрій для вітректомії з пропозицією використати його на їхніх чисельних пацієнтах з травмами очей. Згодом Хейман в Кологні більше захопився вітреохірургією та ми зблизились у Бонні в галузі інтраокулярного мініінвазивного сегментарного склерального пломбування без дренування для відновлення ретинальних відшарувань.
У 1985 році було встановлено, що додаткова вітректомія (нині так звана первинна вітректомія), виконана перед пневматичною ретинопексією, може знижувати високий ризик післяопераційних ускладнень, зумовлених уведенням газу в середину ока.
Первинна вітректомія – 4 операція, що виконується на сьогодні для відновлення первинних відшарувань сітківки. Її мета полягає в зниженні післяопераційної ПВР та зупинці поширення нових розривів після виконання пневматичної ретинопексії. Проте цього не вдалося допоки досягти, оскільки частота розвитку післяопераційної ПВР після первинної вітректомії трималась у межах 11,5 % та після проведення більш сучасних метааналізів залишається на рівні 5,3 %. І, на додаток, відсоток повторних хірургічних втручань після первинної вітректомії становив спочатку 24,5 % та пізніше, з набуттям більшого досвіду та появою нового сучасного обладнання, згідно з даними останнього метааналізу Лінкоффа – близько 13,3 % з прискоренням розвитку катаракти.
Згодом, проаналізувавши ризик співвідношення 3384 інтраокулярних хірургічних втручань проти 1854 екстраокулярних хірургічних маніпуляцій, Харві Лінкофф [30] встановив що: 1) частота виконання повторних операцій після інтраокулярних втручань у 2,5 раза вища, ніж після екстраокулярних; 2) частота післяопераційної ПВР у 6 разів вища після інтраокулярних втручань, ніж після екстраокулярних.
У мультицентрових дослідженнях [31], що проводилися в Європі, порівняли результати виконання первинної вітректомії для відшарувань сітківки середнього ступеня тяжкості після епісклерального пломбування:
– у факічних очах функціональні результати після епісклерального пломбування були кращими, ніж після первинної вітректомії;
– у псевдофакічних очах результати також кращі, але лише за умови наявності циркляжу, після кількох повторних операцій результати обох процедур були порівнянні.
Тому, якщо наявне відшарування сітківки у факічному оці, прогноз є сприятливішим та кількість повторних хірургічних втручань менша після епісклерального пломбування, ніж після первинної вітректомії.
У 2018 році розроблено кілька доступних способів для відновлення первинного гематогенного відшарування сітківки: 2 інтраокулярних та 2 екстраокулярних. Але для досягнення успіху у виконанні будь-якого з них розрив, що підтікає, має бути виявлений та щільно запломбований.
Для кожної з 4 презентованих методик, які можуть бути обрані для відновлення первинного відшарування сітківки, наступні 4 вимоги мають бути дотримані обов’язково:
1) досягнення прилягання сітківки вже після першої операції;
2) досягнення цієї мети шляхом виконання процедури з мінімальними болючими відчуттями;
3) проведення хірургічної методики з мінімальними розхідними витратами та під місцевою анестезією;
4) уникнення появи відтермінованих ускладнень, що можуть поставити під загрозу відновлення зорової функції під час довгострокового спостереження.
ЗАКЛЮЧЕННЯ
Після обговорення розглянутих питань можна дійти висновку, що маятник у хірургії відшарувань, як ми вже мали змогу спостерігати впродовж останніх 85 років, може повертатися знову до екстраокулярної хірургії (у нашому випадку до мінімального сегментарного пломбування без дренування, обмеженого ділянкою розриву та з мінімальними болючими відчуттями). З іншого боку, слід включати як модель лікування мінімальну вітректомію із найменшою кількістю післяопераційних ускладнень, але це після подальшого вдосконалення мікрохірургічних інструментів і техніки самої вітректомії.
Отже, давайте дозволимо собі бути відкритими для нових досягнень, що вже не за горами, у вітреоретинальній хірургії. Водночас потрібно завжди враховувати болючі відчуття, що супроводжують око, та пізні післяопераційні ускладнення, які можуть ставати на заваді відновлення гостроти зору протягом тривалого часу лікування в наших пацієнтів.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
REFERENCES
1. Gonin J. Le traitement opératoire du décollement rétinien. Conférence aux journées médicales de Bruxelles. Bruxelles-Médical. 1930;23:No 17.
2. Guist E. Eine neue Ablatiooperation. ZtschAugenheilk. 1931;74:232–42.
3. Lindner K. Ein Beitrag zur Entstehung und Behandlung der idiopathischen und der traumatischen Netzhautabloesung. Graefes Arch Ophthalmol. 1931;127:177–295.
4. Safar K. Behandlung der Netzhautabhebung mit Elektroden fuer multiple diathermische Stichelung. DtschOphthalmol Ges. 1932;39:119.
5. Rosengren B. Ueber die Behandlung der Netzhautabloesung mittelst Diathermie und Luftinjektion in den Glaskoerper. Acta Ophthalmol. 1938;16:3–42.
6. Schepens CL. Prognosis and treatment of retinal detachment. The Mark J Schoenberg Memorial Lecture. A review by Kronenberg B, New York Society for Clinical Ophthalmology. Am J Ophthalmol. 1953;36:1739–56.
7. Pruett RC. The fishmouth phenomenon: II. Wedge scleral buckling. Arch Ophthalmol. 1977;95(10):1782–7.
8. Custodis E. Bedeutet die Plombenaufnaehung auf die Sklera einen Fortschritt in der operativen Behandlung der Netzhautablösung? Berichte der Deutschen Ophthalmologischen Gesellschaft. 1953;58:102–5.
9. Lincoff H, Baras I, McLean J. Modifications to the Custodis procedure for retinal detachment. Arch Ophthalmol. 1965;73:160–3.
10. Lincoff H, O’Connor P, Kreissig I. Die Retina-Adhaesion nach Kryopexie. Klin Monatsbl Augenheilkd. 1970;156:771–83.
11. Kreissig I, Lincoff H. Ultrastruktur der Kryopexieadhäsion. In: DOG Symp. “Die Prophylaxe der idiopathischen Netzhautabhebung”. Bergmann, München, 1971:191–205.
12. Kreissig I, Lincoff H. Mechanism of retinal attachment after cryosurgery. Trans Ophthalmol Soc UK. 1975;95:148–57.
13. Lincoff H, Gieser R. Finding the retinal hole. Arch Ophthalmol. 1971;85:565–9.
14. Lincoff H, Kreissig I. Extraocular repeat surgery of retinal detachment. A minimal approach. Ophthalmology. 1996;103:1586–92.
15. Lincoff H, Kreissig I. Advantages of radial buckling. Am J Ophthalmol. 1975;79:955–7.
16. Kreissig I, Rose D, Jost B. Minimized surgery for retinal detachments with segmental buckling and nondrainage. An 11-year follow-up. Retina. 1992;12:224–31.
17. Kreissig I, Simader E, Fahle M, Lincoff H. Visual acuity after segmental buckling and nondrainage: a 15-year follow-up. Eur J Ophthalmol. 1995;5:240–6.
18. Lincoff HA, Kreissig I, Hahn YS. A temporary balloon buckle for the treatment of small retinal detachments. Ophthalmology. 1979;86:586–92.
19. Kreissig I, Failer J, Lincoff H, Ferrari F. Results of a temporary balloon buckle in the treatment of 500 retinal detachments and a comparison with pneumatic retinopexy. Am J Ophthalmol. 1989;107:381–9.
20. Norton EWD. Intraocular gas in the management of selected retinal detachments. Trans Am Acad Ophthalmol Otolaryngol. 1973;77:85–98.
21. Lincoff H. Reply to Drs Fineberg, Machemer, Sullivan and Norton. Mod Probl Ophthalmol. 1974;12:344–5.
22. Kreissig I. Clinical experience with SF6-gas in detachment surgery. Berichte der Deutschen Ophthalmologischen Gesellschaft. 1979;76:553–60.
23. Kreissig I, Stanowsky A, Lincoff H, Richard G. Treatment of difficult retinal detachments with expanding gas bubble without vitrectomy. Graefe’s Arch. Clin. Exp. Ophthalmol. 1986;224:51–4.
24. Kreissig I. The expanding-gas operation after 15 years: Data of animal experiments, subsequent modifications of the procedure and clinical results in the treatment of retinal detachments. Klin Mbl Augenheilk. 1990;197:231–9.
25. Lincoff A, Haft D, Liggett P, Reifer C. Intravitreal expansion of perfluorocarbon bubbles. Arch Ophthalmol. 1980;98;1646.
26. Lincoff H, Maisel JM, Lincoff A. Intravitreal disappearance rates of four per-fluorocarbon gases. Arch Ophthalmol. 1984;102:928–9.
27. Dominguez A, Fonseca A, Gomez-Montana J. Gas tamponade for ambulatory treatment of retinal detachment. In: Proceedings of the XXVth International Congress of Ophthalmology. Rome, May 4–10, 1986. Kugler&Ghedini, Amsterdam; 1987:2038–45.
28. Hilton GF, Grizzard WS. Pneumatic retinopexy. A two-step outpatient operation without conjunctival incision. Ophthalmology. 1986;93:626–41.
29. Machemer R, Buettner H, Norton EWD, Parel JM. Vitrectomy: a pars plana approach. Trans Am Acad Ophthalmol. 1971;75:813–20.
30. Lincoff H, Lincoff A, Stopa M. Systematic review of efficacy and safety of surgery for primary retinal detachment. In: Kreissig I, editor. Primary retinal detachment: Options for repair. Chapter 8. Springer; 2004. p. 161–75.
31. Heimann H, Bartz-Schmidt KU, Bornfeld N, Weiss C, Hilgers RD, Foerster MH. Scleral buckling versus primary vitrectomy in rhegmatogenous retinal detachment: a prospective randomized multicenter clinical study. Ophthalmology. 2008;115:1634–5.
Переклад з англійської мови.
Для цитування:
Kreissig I. Repair of Primary Retinal Detachment:
Review of Techniques for Repair Developed in the
Past 85 Years. International Scientific-Practical Journal
Ophthalmology. 2018;1(08):68–83.
https://doi.org/10.30702/Ophthalmology.2018/08.06